Что такое импорт и экспорт контактов в телефоне
Люди часто сталкиваются с необходимостью переноса контактных данных между сотовыми. Чтобы не добавлять каждую запись заново и по отдельности предусмотрены функции экспорта и импорта. Иногда потребители путают эти понятия. Статья поможет разобраться, чем различаются два термина, и покажет, как совершаются такие процессы в современных смартфонах.
Что значит импорт и экспорт контактов в телефоне
Говоря простым языком, импорт — это добавление, а экспорт — изъятие.
Что такое импорт и зачем он нужен
Импорт — добавление контактных данных в приложение на девайсе с внутреннего хранилища, SIM- или MicroSD-карты.
Нужен он при смене пользователем мобильного устройства и необходимости перенести значения с SIM-карты. Этот процесс находит применение при восстановлении данных с резервной копии.
Экспорт и его функции
Экспортом называется перенос контактных данных на мобильном девайсе во внутренний или внешний накопитель либо на SIM-карту.
Основными его функциями являются перемещение текстовой информации между сотовыми либо на SIM-карту и создание Backup’а (резервной копии). Процесс бывает полезен при освобождении места на накопителе. Но это актуально лишь для старых сотовых, где максимальное количество имен в телефонной книге небольшое.
В чем ключевые отличия импорта от экспорта
Импорт и экспорт контактов в телефоне отличаются тем, что в первом происходит добавление информации в список номеров, а во втором сведения, наоборот, изымаются оттуда. Разница в том, что экспортировать данные обычно означает записать текст в память девайса, а импортировать контакты — это значит считать сведения с файла, находящегося на устройстве.
Как экспортировать и импортировать контакты
Экспортировать или импортировать контакты на Android-устройствах можно несколькими способами. Первый — через стандартное приложение «Контакты» на телефоне, второй — используя сторонний софт.
Используя Google-аккаунт
Перенести номера на аккаунт Google можно таким образом:
- Открыть «Контакты» на устройстве.

- Тапнуть на значок «Меню».
- Выбрать «Настройки» и «Экспорт контактов».
- Указать место для передачи сведений.
- Коснуться «Экспортировать в VCF-файл» или «Сохранить».
Внимание! Добавить данные на девайсах с ОС Android можно с SIM-карты или виртуальной карточки, находящейся в памяти аппарата.
Для извлечения с SIM понадобится произвести следующие действия:
- Вставить СИМ-карту в смартфон или планшет.
- Открыть программу, содержащую номера на Android-устройстве.
- Коснуться значка «Меню».
- Тапнуть «Настройки», «Импорт контактов».
- Нажать на пункт «SIM-карта» (в некоторых версиях ОС предлагает выбор оператора). Указать аккаунт для сохранения материала.
Если сведения находятся в специальном документе формата .vcf, импорт производится так:
- Перейти в приложение «Контакты».

- Произвести нажатие на виртуальную кнопку «Меню» в левом верхнем углу экрана.
- Затем на «Настройки» и «Импорт контактов».
- Выбрать «VCF-файл». Из предложенных аккаунтов указать тот, где требуется сохранить контактные данные.
- Найти и открыть документ .vcf, откуда будут извлечены значения.
Через сторонние приложения
Перенос информации с мобильных устройств можно осуществить с помощью компьютерной программы MOBILedit.
Экспортировать контакты с помощью MOBILedit можно следующим образом:
- В самой программе перейти на вкладку «Телефон/Phones», далее указать «Соединение/Connection Wizars» (в последней версии утилиты кнопка доступна на стартовой вкладке).
- В появившемся окне выбрать PC Sync или Cable (в зависимости от версии программы).
- Перейти в настройки мобильного телефона и кликнуть на пункт «Система» или «Расширенные настройки».

- Выбрать строку «Для разработчиков».
- Если этой надписи нет, открыть пункт «О телефоне» и тапнуть несколько раз на «Номер сборки» или «Версия MIUI» до появления соответствующего уведомления.
- После этого в настройках для разработчиков включить «Отладку по USB».
- Теперь с ПК кликнуть на пункт «Phonebook», находящийся на панели MOBILedit’а.
- Выбрать, какие именно нужно экспортировать контакты.
- Выбрав контакты, нажать кнопку «Экспорт/Export».
- Указать тип файла CSV и путь сохранения его на компьютере.
Импортировать контакты в данной утилите ещё проще. Требуется совершить следующие действия:
- Подключить смартфон к компьютеру.
- Открыть пункт «Импорт/Import» в программе MOBILedit.
- Выбрать файл, полученный при экспорте, и кликнуть на «Import».
Достоинствами программы MOBILedit являются поддержка большого количества моделей телефонов (не только смартфонов с ОС Android) и возможность экспорта в CSV-файл, который беспрепятственно открывается в Microsoft Excel. Но у приложения есть и недостатки: отсутствие русского языка и платная лицензия.
Но у приложения есть и недостатки: отсутствие русского языка и платная лицензия.
Секретный экспорт за январь – июнь вырос на 61% до $27 млрд
Как мы считали
Основной источник данных – таможенная статистика внешней торговли РФ, а также данные ООН Comtrade и национальные базы по внешней торговле.
ФТС публикует статистику по внешнему торговому обороту России в разрезе разных товарных категорий. Получить данные можно по укрупненным группам товаров и отдельным позициям. На первом – максимально общем – уровне детализации товарам присваивается двузначный код. На следующем этапе степень детализации растет. Этот уровень предполагает четырехзначный код: первые два знака означают укрупненную группу, вторые – более узкую категорию. Например, на первом уровне детализации по группе 07 «Овощи» ФТС приводит данные по всему спектру овощей. На следующем – четырехзначном – уровне таможня публикует статистику по более конкретной позиции в рамках группы 07. Например, 0701 – «Картофель свежий или охлажденный». В общей сложности ФТС приводит данные по пяти ступеням, максимальный уровень детализации – 10 знаков.
Например, 0701 – «Картофель свежий или охлажденный». В общей сложности ФТС приводит данные по пяти ступеням, максимальный уровень детализации – 10 знаков.
Два знака
Тем не менее ФТС приводит в своей статистике данные не по всем группам и позициям. Значения по некоторым категориям экспорта и импорта публикуются под специальными кодами – SS, SSSS и так далее вплоть до 10 знаков. Это означает, что торговля этими товарами засекречена. Сравнительный анализ таможенной статистики позволяет выявить, какие именно товары попадают в данные под секретными кодами.
В общей сложности в ТН ВЭД включено 97 укрупненных групп товаров. Но конкретные значения экспорта и импорта приводятся по 95. Остаток публикуется под секретным кодом SS. Данные не приводятся по двум группам – 88 «Летательные аппараты, космические аппараты и их части», а также 93 «Оружие и боеприпасы». Это позволяет сделать вывод, что именно они публикуются под секретным кодом. К тому же торговлю с другими странами по обеим группам товаров Россия ведет – частично суммы экспорта по категориям 88 и 93 приводятся в базе данных ООН Comtrade.
Четыре знака
На четырехзначном уровне появляются дополнительные отдельные секретные позиции. Кроме всех подгрупп в укрупненных категориях 88 и 93 закрываются данные по позициям «Изотопы» (группа 2845), «Танки и БТР» (8710), «Детские коляски» (8715) и «Суда, лодки, плавучие конструкции» (8906). Такой вывод можно сделать, сопоставив показатели торговли по двузначной группе и суммы значений по позициям с четырехзначным кодом, включенным в эту группу. Если показатели не совпадают, то это может означать с высокой степенью вероятности, что часть позиций с четырехзначным кодом засекречивается. Например, экспорт по категории 28 был $2,37 млрд, а в сумме по всем подгруппам 2801, 2802 и т. д. – только $1,69 млрд, значит, часть данных перенесена в секретную часть (SSSS). В группе 28 есть данные по всем подгруппам, кроме 2845 и 2848. Это может означать, что именно они и засекречены.
Шесть и восемь знаков
Аналогичным способом анализировалась статистика при продвижении вглубь по дереву ТН ВЭД – до шести-, восьмизначных кодов и т.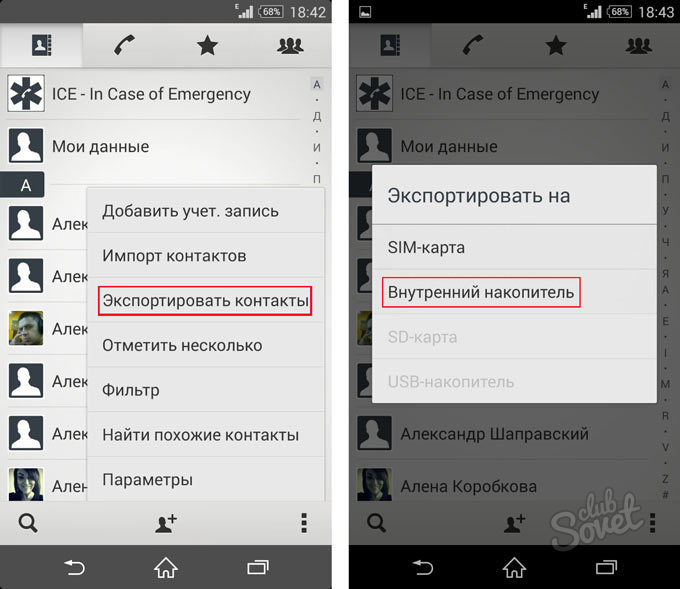 д.
д.
На уровне шести знаков (SSSSSS) секретным становится природный газ в газообразном состоянии (подгруппа 2711 21) и частично – СПГ (2711 11).
На следующей ступени – восьмизначном уровне – ФТС полностью закрыла поставки в Иран. При дальнейшем продвижении по дереву ТН ВЭД – до 10 знаков – общая сумма засекреченной торговли аналогична показателями, отраженным в восьмизначной торговле (SSSSSSSS).
Аналогичную методику определения, какие товары попадают в секретные категории, приводил ранее РБК.
В ФТС «Ведомостям» сообщили, что в таможенную статистику попадают все данные о внешней торговле со всеми странами без исключения и неучтенных категорий нет.
Нетто — экспортер — Что такое Нетто — экспортер?
23152
Так обычно называют страну, которая экспортирует больше продукции, товаров и услуг больше, чем импортирует.
Нетто — экспортером обычно называют страну, которая экспортирует больше продукции, товаров и услуг больше, чем импортирует.
И напротив, если страна импортирует больше, чем экспортирует, то она становится нетто — импортером.
К примеру, США в последние 30-40 лет импортирует больше, чем экспортирует, поэтому является нетто — импортером.
Превышение экспорта над импортом повышает уровень ВВП страны, что обеспечивает рост экономики.
Есть объективные причины необходимости импорта.
К примеру, если в стране недостаточно запасов углеводородных ресурсов, их вынужденно импортируют. К примеру, США до недавнего времени были нетто — импортерами углеводородов и, при этом , имели самую развитую экономику в мире.
Стратегия США была — в сохранении природных ископаемых.

С приходом к власти президента — бизнесмена Д. Трампа , предвыборный лозунг которого — сделать Америку снова великой, бурный рост добычи продолжился.
Импортируемые ресурсы являются двигателем для развития многих отраслей промышленности в развитых странах.
Если в стране слабая валюта, ее экспорт, как правило, более конкурентоспособен на международных рынках, что стимулирует положительный чистый экспорт.
И наоборот, если в стране сильная валюта, ее экспорт обходится дороже, и внутренние потребители могут покупать иностранный экспорт по более низкой цене, что может привести к отрицательному чистому экспорту.
A1 — Перенос контактов SIM-карты —
При замене SIM/USIM-карты на новую необходимо сохранить контакты с SIM-карты в телефон, а после установки новой SIM/USIM скопировать из телефона.
Общие особенности копирования зависят от операционной системы.
Ниже представлены примеры для смартфонов с ОС Android 4.2.2, 5.0.1, 7.1.2, 8.0.0, iOS, Windows Phone 10, а также для кнопочных телефонов на примере Sony Ericsson W890i и Alcatel One Touch 20 00X.
| Android | iOS | Windows Phone 10 | |
|---|---|---|---|
Место расположения пунктов меню для копирования контактов смартфонов различных производителей могут различаться. Например, для переноса контактов в: | В смартфонах с iOS перенести контакты можно непосредственно с SIM-карты на смартфон (без возможности копирования с SIM на SIM/USIM). | Место расположения пунктов меню для копирования контактов телефонов различных производителей могут различаться. Например, для переноса контактов в: | В смартфонах с Windows Phone 10 перенести контакты можно непосредственно с SIM-карты на смартфон (без возможности копирования с SIM на SIM/USIM). |
| Samsung с Android 5.0.1: Зайдите в Меню –> Телефон (он же программа для звонков), Выберите Настройки –> Затем Контакты-> Затем Импорт/экспорт контактов Выберите «Импортировать с SIM-карты» или «Экспортировать на SIM-карту» | Зайдите в Настройки –> Контакты –> Выберите пункт «Импортировать контакты SIM» | Sony Ericsson W890i: Зайдите в Контакты –> Функции –> Доп. 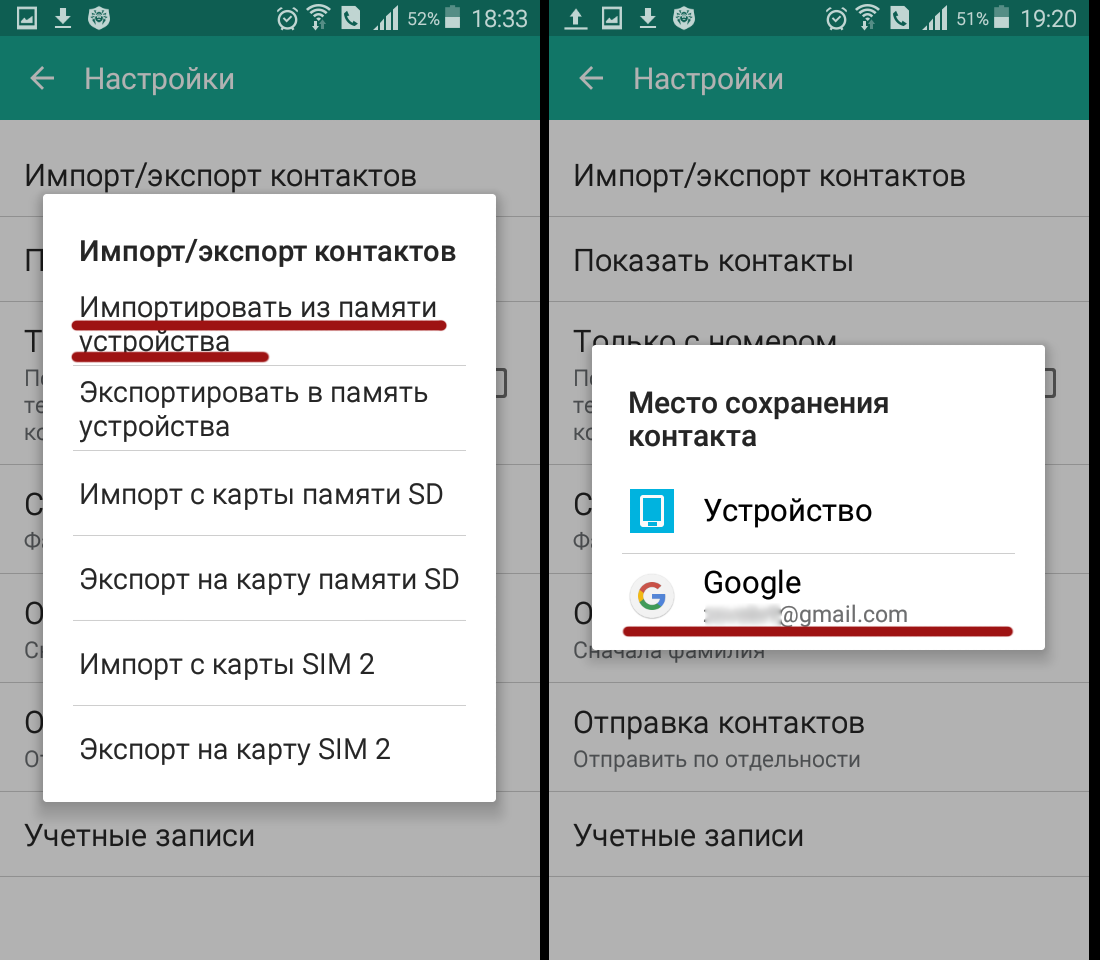 функции –> функции –>Дополнительно –> Скопировать с SIM/ Скопировать на SIM Alcatel One Touch 20 00X: | Зайдите в Меню –> Люди. Нажмите «Импорт с SIM-карты» |
| Samsung c Android 8.0.0: Зайдите в Меню –> Контакты Нажмите вверху справа три точки и выберите Управление Контактами –> Импорт/экспорт контактов Выберите «Импорт» и «Экспорт» | |||
| Huawei c Android 4.2.2: Зайдите в Контакты –> три точки внизу –> Импорт/экспорт контактов | |||
Xiaomi с Android 7. 1.2: 1.2:Зайдите в Меню -> Контакты –> Нажмите три точки, выберите «Импорт» или «Экспорт» Затем выберите, куда и откуда экспортировать\импортировать контакты |
| Android | iOS | Кнопочный телефон | Windows Phone 10 |
|---|---|---|---|
| Место расположения пунктов меню для копирования контактов смартфонов различных производителей могут различаться. Например, для переноса контактов в: | В смартфонах с iOS перенести контакты можно непосредственно с SIM-карты на смартфон (без возможности копирования с SIM на SIM/USIM). | Место расположения пунктов меню для копирования контактов телефонов различных производителей могут различаться. Например, для переноса контактов в: | В смартфонах с Windows Phone 10 перенести контакты можно непосредственно с SIM-карты на смартфон (без возможности копирования с SIM на SIM/USIM). |
| Samsung с Android 5.0.1: Зайдите в Меню → Телефон (он же программа для звонков), Выберите Настройки → Затем Контакты → Затем Импорт/экспорт контактов Выберите «Импортировать с SIM-карты» или «Экспортировать на SIM-карту» | Зайдите в Настройки → Контакты → Выберите пункт «Импортировать контакты SIM» | Sony Ericsson W890i: Зайдите в Контакты → Функции → Доп. функции → Дополнительно → Скопировать с SIM/ Скопировать на SIM Alcatel One Touch 20 00X: | Зайдите в Меню → Люди. Нажмите «Импорт с SIM-карты» |
| Samsung c Android 8.0.0: Зайдите в Меню → Контакты Нажмите вверху справа три точки и выберите Управление Контактами → Импорт/экспорт контактов Выберите «Импорт» и «Экспорт» | |||
| Huawei c Android 4.2.2: Зайдите в Контакты → три точки внизу → Импорт/экспорт контактов | |||
| Xiaomi с Android 7.1.2: Зайдите в Меню → Контакты → Нажмите три точки, выберите «Импорт» или «Экспорт» Затем выберите, куда и откуда экспортировать\импортировать контакты |
Не удается найти страницу | Autodesk Knowledge Network
(* {{l10n_strings.REQUIRED_FIELD}})
{{l10n_strings.CREATE_NEW_COLLECTION}}*
{{l10n_strings. ADD_COLLECTION_DESCRIPTION}}
ADD_COLLECTION_DESCRIPTION}}
{{l10n_strings.DRAG_TEXT_HELP}}
{{l10n_strings.LANGUAGE}} {{$select.selected.display}}{{article. content_lang.display}}
content_lang.display}}
{{l10n_strings.AUTHOR_TOOLTIP_TEXT}}
{{$select.selected.display}} {{l10n_strings.CREATE_AND_ADD_TO_COLLECTION_MODAL_BUTTON}} {{l10n_strings.CREATE_A_COLLECTION_ERROR}}Как сделать экспорт/импорт каталога товаров?
Возможный результат:Вот так может выглядеть ваш каталог товаров в формате csv.
Использование:
С помощью данной опции вы сможете быстро и просто управлять каталогом товаров через редактирование csv-файла в Excel. Загрузите новые товары (или каталог товаров целиком) или измените уже существующие: цены, описание, наличие, скидки и многое другое.
Преимущества:
- Быстрое редактирование структуры каталога товаров.
- Массовое редактирование товаров.
- Быстрая загрузка новых данных.
- У вас всегда будет копия вашего каталога товаров.
Рекомендуется всем интернет-магазинам.
Подключение:
1. Перейдите раздел «Настройки» — «Магазин» — «Экспорт/импорт».
2. Чтобы выгрузить каталог товаров на свой компьютер, в блоке «Экспорт каталога» нажмите кнопку «Начать экспорт», подождите некоторое время и нажмите кнопку «Обновить для получения ссылки». Формирование файла может занять несколько минут, в зависимости от количества позиций в каталоге товаров.
3. Чтобы загрузить файл со своего компьютера на сайт, в блоке «Импорт каталога» нажмите кнопку «Выбрать файл .CSV» и выберите необходимый файл. Загрузка данных может занять несколько минут, в зависимости от количества позиций в каталоге товаров. Чтобы проверить окончание процесса, нажмите кнопку «Проверить окончание импорта». Если все прошло хорошо, то вы увидите сообщение «Каталог товаров обновлен».
Важно!
На бесплатном тарифе «Старт» доступно 10 товаров. На тарифе «Сайт» — 10 товаров.
Чтобы выгрузить до 50 товаров — нужно подключить тариф «Мастер».
Чтобы выгрузить все товары — тариф «Бизнес» или «Магазин».
Если во время импорта файла .CSV вы получаете ошибку, посмотрите, в какой она строке, и исправьте.
Также читайте:
Была ли статья вам полезна? Да Нет
2021 год стал для «Газпрома» рекордным – Новости ТЭК Кубани
Получены оперативные данные по итогам работы компании за 2021 год. Он стал для «Газпрома» рекордным.
Он стал для «Газпрома» рекордным.
В 2021 году мы добыли 514,8 млрд куб. м газа. Это лучший результат за последние 13 лет. И это плюс 62,2 млрд куб. м к показателю 2020 года. Прирост добычи «Газпрома» покрыл львиную долю роста мирового потребления газа в 2021 году.
Как и всегда, мы обеспечили надежное газоснабжение потребителей. По предварительной информации, на российский рынок из газотранспортной системы «Газпром» поставил 257,8 млрд куб. м газа. Это максимальный уровень с 2013 года. Рост по сравнению с 2020 годом — на 31,9 млрд куб. м газа.
В страны дальнего зарубежья мы экспортировали 185,1 млрд куб. м газа — на 5,8 млрд куб. м больше, чем в 2020 году. Результат 2021 года занял четвертую строчку среди исторических рекордов компании. Отмечу, что закупку российского трубопроводного газа нарастили 15 стран. Самый большой прирост обеспечили его крупнейшие потребители — Германия (+10,5%), Турция (+63%), Италия (+20,3%).
Значительную роль в обеспечении надежных поставок российского газа в Европу играют современные морские газопроводы «Северный поток» и «Турецкий поток». Поэтому особенно важно, что с 29 декабря прошлого года полностью готов к работе еще один морской газопровод — «Северный поток — 2», с проектной мощностью 55 млрд куб. м газа в год.
Поэтому особенно важно, что с 29 декабря прошлого года полностью готов к работе еще один морской газопровод — «Северный поток — 2», с проектной мощностью 55 млрд куб. м газа в год.
Растет экспорт газа по газопроводу «Сила Сибири» в КНР. На протяжении 2021 года мы регулярно поставляли газ в Китай с превышением контрактных обязательств. С 1 января 2022 года «Газпром» вышел на новый уровень поставок, как это и предусмотрено долгосрочным двусторонним договором купли-продажи газа.
Мы перевыполнили планы по реализации в 2021 году нашего главного социального проекта — развитие газификации российских регионов. Построили около 2,7 тыс. км газопроводов. Возможность подключения к газу получили жители 342 населенных пунктов по всей стране. Масштабная газификация продолжается. Планы-графики синхронизации работ на 2022 год между «Газпромом» и субъектами РФ подписаны.
По итогам 2021 года мы ожидаем максимальный за всю историю «Газпрома» финансовый результат. А это значит, что дивиденды также будут абсолютно рекордными — причем как для «Газпрома», так и среди всех российских публичных компаний.
Страхование экспортных кредитов
Страхование экспортных кредитов (ECI) защищает экспортера товаров и услуг от риска неплатежа иностранным покупателем. Другими словами, ECI значительно снижает платежные риски, связанные с ведением бизнеса на международном уровне, предоставляя экспортеру условную гарантию того, что платеж будет произведен, если иностранный покупатель не сможет заплатить. Проще говоря, экспортеры могут защитить свою иностранную дебиторскую задолженность от различных рисков, которые могут привести к неплатежу со стороны иностранных покупателей.
ECI обычно покрывает коммерческие риски (такие как неплатежеспособность покупателя, банкротство или затяжные дефолты/медленные платежи) и определенные политические риски (такие как война, терроризм, беспорядки и революция), которые могут привести к неуплате. ECI также охватывает неконвертируемость валюты, экспроприацию и изменения правил импорта или экспорта. ECI предлагается либо на основе одного покупателя, либо на основе портфеля нескольких покупателей на краткосрочные (до одного года) и среднесрочные (от одного до пяти лет) периоды погашения.
ECI предлагается либо на основе одного покупателя, либо на основе портфеля нескольких покупателей на краткосрочные (до одного года) и среднесрочные (от одного до пяти лет) периоды погашения.
Ключевые моменты
ECI позволяет экспортерам предлагать иностранным покупателям конкурентоспособные условия открытого счета, сводя к минимуму риск неплатежа.
Даже платежеспособные покупатели могут не платить по независящим от них обстоятельствам.
Снизив риск неплатежей, экспортеры могут увеличить экспортные продажи, занять долю рынка в странах с формирующимся рынком и развивающихся странах и более активно конкурировать на мировом рынке.

Когда иностранная дебиторская задолженность застрахована, кредиторы более склонны увеличивать кредитоспособность экспортера и предлагать более привлекательные условия финансирования.
ECI не покрывает физическую утрату или повреждение товаров, отгруженных покупателю, а также любые риски, которые покрываются посредством морского страхования, страхования от пожара, страхования от несчастных случаев или других форм страхования.
Применимость
Рекомендуется для использования в сочетании с условиями открытого счета и предэкспортным финансированием оборотного капитала.
Риск
Экспортеры принимают на себя риск непокрытой части убытков, и их претензии могут быть отклонены в случае несоблюдения требований, указанных в полисе.
Pros
Снижает риск неплатежа иностранными покупателями, предлагает безопасные условия открытого счета на мировом рынке.
Минусы
Стоимость получения и поддержания страхового полиса. Разделение риска в виде франшизы (покрытие обычно ниже 100 процентов).
Покрытие
Краткосрочная ECI, которая обеспечивает покрытие от 90 до 95 процентов коммерческих и политических рисков, которые приводят к неплатежу покупателя, обычно покрывает (a) потребительские товары, материалы и услуги на срок до 180 дней и (b) мелкие капитальные товары, потребительские товары длительного пользования и оптовые товары до 360 дней. Среднесрочная ECI, которая обеспечивает 85-процентное покрытие чистой стоимости контракта, обычно покрывает крупное капитальное оборудование на срок до пяти лет. ECI, стоимость которой экспортеры часто включают в цену продажи, должна быть упреждающей покупкой, поскольку экспортеры должны получить покрытие до того, как клиент станет проблемой.
Среднесрочная ECI, которая обеспечивает 85-процентное покрытие чистой стоимости контракта, обычно покрывает крупное капитальное оборудование на срок до пяти лет. ECI, стоимость которой экспортеры часто включают в цену продажи, должна быть упреждающей покупкой, поскольку экспортеры должны получить покрытие до того, как клиент станет проблемой.
Где я могу получить страховку экспортного кредита?
Полисы ECI предлагаются многими частными компаниями по страхованию коммерческих рисков, а также Экспортно-импортным банком США (EXIM), государственным агентством, которое помогает финансировать экспорт товаров и услуг США на международные рынки. Американским экспортерам настоятельно рекомендуется обращаться к специализированному страховому брокеру, который может помочь им выбрать наиболее экономически эффективное решение для их нужд.Уважаемые, хорошо зарекомендовавшие себя компании, которые продают коммерческие полисы ECI, можно легко найти в Интернете. Вы также можете купить полисы ECI непосредственно у EXIM. Кроме того, список активных страховых брокеров, зарегистрированных в EXIM, доступен на сайте www.exim.gov, или вы можете позвонить по телефону 1-800-565-EXIM (3946) для получения дополнительной информации.
Вы также можете купить полисы ECI непосредственно у EXIM. Кроме того, список активных страховых брокеров, зарегистрированных в EXIM, доступен на сайте www.exim.gov, или вы можете позвонить по телефону 1-800-565-EXIM (3946) для получения дополнительной информации.
Страхование экспортных кредитов частного сектора
Премии определяются индивидуально на основе факторов риска и могут быть снижены для известных и опытных экспортеров.
Стоимость большинства полисов с несколькими покупателями составляет менее 1 процента от застрахованных продаж, в то время как цены на полисы с одним покупателем сильно различаются из-за предполагаемого более высокого риска.

Нет ограничений в отношении иностранного контента или военных продаж.
Коммерческие страховые компании обычно могут предлагать гибкие и дискреционные кредитные лимиты.
Страхование экспортных кредитов EXIM Bank
Клиентам EXIM рекомендуется обратиться к разделу «Информация о плате за риск и калькуляторы комиссии» (которые размещены на веб-сайте Банка www.
 exim.gov в разделе «Применить»), чтобы определить комиссионные сборы (премии).
exim.gov в разделе «Применить»), чтобы определить комиссионные сборы (премии).Покрытие доступно на более рискованных развивающихся зарубежных рынках, где частные страховщики могут не работать.
Экспортеры, выбравшие гарантию оборотного капитала EXIM, могут получить 25-процентную скидку на страховые полисы для нескольких покупателей.
Предлагается усиленная поддержка экологически благоприятного экспорта.

Продукты должны быть доставлены из США и содержать не менее 50 процентов U.С. содержание.
EXIM не может поддерживать товары военного назначения или закупки, сделанные иностранными военными организациями.
Поддержка экспорта может быть прекращена или ограничена в некоторых странах по причинам политики правительства США (дополнительную информацию см.
 в Графике ограничений по странам, размещенном на веб-сайте Банка в разделе «Применить»).
в Графике ограничений по странам, размещенном на веб-сайте Банка в разделе «Применить»).
Эта статья взята из главы 9 Руководства по торговому финансированию правительства США.Чтобы узнать больше о страховании кредита, посетите веб-сайт EXIM.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера для приема файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались.
 Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie. - Ваш браузер не поддерживает файлы cookie. Попробуйте другой браузер, если вы подозреваете это.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы это исправить, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Индия возобновляет экспорт вакцины по мере накопления внутренних запасов – официальные лица в Ахмедабаде, Индия, 28 сентября 2021 г. REUTERS/Amit Dave
Зарегистрируйтесь сейчас и получите БЕСПЛАТНЫЙ неограниченный доступ к Reuters.com
Зарегистрируйтесь
НЬЮ-ДЕЛИ, 13 октября (Рейтер) — Индия возобновила небольшой объем экспорта COVID -19 вакцин и значительно увеличит экспорт в ближайшие несколько месяцев по мере накопления внутренних запасов и вакцинации большей части населения страны, заявили официальные лица в среду.
Один миллион инъекций Covaxin производства индийской компании Bharat Biotech был отправлен на прошлой неделе в Иран, сообщило посольство Индии в Тегеране.
Вакцины также были отправлены в Непал, сообщил источник в правительстве, добавив, что усилия сосредоточены на соседних странах.
Зарегистрируйтесь сейчас и получите БЕСПЛАТНЫЙ неограниченный доступ к Reuters.com
Зарегистрируйтесь
На данный момент было экспортировано около 4 миллионов прививок, сообщил источник, что является небольшим количеством по сравнению с обширной вакцинной дипломатией, которую правительство премьер-министра Нарендры Моди начало в этом году. вторая волна инфекций заставила остановиться.
Но теперь, когда три четверти взрослого населения получили одну прививку, а треть – обе, Индия готова сыграть важную роль в удовлетворении потребностей зарубежных стран в вакцинах, сказал В. К. Пол, возглавляющий правительственную целевую группу по COVID-19.
К. Пол, возглавляющий правительственную целевую группу по COVID-19.
«Поскольку потребности Индии будут удовлетворены, в будущем у нас будет большой запас вакцин», — сказал Пол журналистам.
Институт сывороток производит 220 миллионов прививок вакцины Oxford AstraZeneca в месяц по сравнению со 150 миллионами в августе, а Bharat Biotech поставляет 30 миллионов прививок своей собственной вакцины, количество которых в следующем месяце увеличится до 50 миллионов. он сказал.
В связи с тем, что несколько других местных вакцин приближаются к производству или получают одобрение регулирующих органов, Индия, как ожидается, будет производить 300-320 миллионов прививок в месяц к началу следующего года — больше, чем в среднем 210 миллионов доз, которые она вводит своим людям каждую Месяц», — заявили чиновники.
«В следующем году можно визуализировать огромную, огромную доступность вакцин, мы ожидаем, что вакцины, произведенные в Индии, сыграют значительную роль в борьбе с пандемией во всем мире», — сказал Пол.
Индия является крупнейшим в мире производителем вакцин. Пол сказал, что в ближайшие два-три дня компания преодолеет отметку в 1 миллиард доз вакцины, введенных с начала ее массовой кампании по вакцинации всех взрослых индийцев.
Зарегистрируйтесь сейчас и получите БЕСПЛАТНЫЙ неограниченный доступ к Reuters.com
Зарегистрируйтесь
Репортаж Санджива Миглани; Под редакцией Тимоти Херитэдж
Наши стандарты: Принципы доверия Thomson Reuters.
Локализация нуклеопорина Tpr в комплексе ядерных пор необходима для опосредованной Tpr регуляции экспорта несплайсированной РНК
Abstract
Нуклеопорин Tpr является компонентом комплекса ядерных пор (NPC), локализованным исключительно во внутриядерных филаментах.Tpr функционирует как каркасный элемент в ядерной фазе NPC и играет роль в передаче сигналов контрольной точки митотического веретена. Экспорт интрон-содержащей мРНК в вирусе обезьян Mason Pfizer регулируется прямым взаимодействием клеточных белков с -цис--действующим конститутивным транспортным элементом (CTE). В клетках млекопитающих транспорт репортерной конструкции Gag/Pol-CTE не очень эффективен, что указывает на регуляторный механизм сохранения этой несплайсированной РНК. Здесь мы сообщаем, что нокдаун Tpr в клетках млекопитающих приводит к резкому увеличению уровней белков Gag (p24) в цитоплазме, что восстанавливается с помощью Tpr, устойчивого к siRNA.Роль Tpr в сохранении несплайсированной РНК не зависит от функций белков Sam68 и Tap/Nxf1, которые, как сообщается, способствуют CTE-зависимому экспорту. Кроме того, мы исследовали возможную роль нуклеопоринов, которые, как известно, функционируют в ядерно-цитоплазматическом транспорте, в модуляции экспорта несплайсированной РНК. Результаты показывают, что истощение Nup153, нуклеопорина, необходимого для закрепления Tpr на NPC, играет роль в регуляции экспорта, в то время как истощение других нуклеопоринов, содержащих повторы FG, не изменяет экспорт несплайсированной РНК.Результаты показывают, что Tpr и Nup153 оба регулируют экспорт несплайсированной РНК, и они, скорее всего, функционируют одним и тем же путем.
В клетках млекопитающих транспорт репортерной конструкции Gag/Pol-CTE не очень эффективен, что указывает на регуляторный механизм сохранения этой несплайсированной РНК. Здесь мы сообщаем, что нокдаун Tpr в клетках млекопитающих приводит к резкому увеличению уровней белков Gag (p24) в цитоплазме, что восстанавливается с помощью Tpr, устойчивого к siRNA.Роль Tpr в сохранении несплайсированной РНК не зависит от функций белков Sam68 и Tap/Nxf1, которые, как сообщается, способствуют CTE-зависимому экспорту. Кроме того, мы исследовали возможную роль нуклеопоринов, которые, как известно, функционируют в ядерно-цитоплазматическом транспорте, в модуляции экспорта несплайсированной РНК. Результаты показывают, что истощение Nup153, нуклеопорина, необходимого для закрепления Tpr на NPC, играет роль в регуляции экспорта, в то время как истощение других нуклеопоринов, содержащих повторы FG, не изменяет экспорт несплайсированной РНК.Результаты показывают, что Tpr и Nup153 оба регулируют экспорт несплайсированной РНК, и они, скорее всего, функционируют одним и тем же путем. Важно отметить, что мы обнаружили, что локализация Tpr в NPC необходима для опосредованной Tpr регуляции экспорта несплайсированной РНК. В совокупности данные указывают на то, что перинуклеарная локализация Tpr в нуклеопорном комплексе имеет решающее значение для регуляции экспорта мРНК, содержащей интрон, путем прямого или косвенного участия в процессинге и деградации аберрантных транскриптов мРНК.
Важно отметить, что мы обнаружили, что локализация Tpr в NPC необходима для опосредованной Tpr регуляции экспорта несплайсированной РНК. В совокупности данные указывают на то, что перинуклеарная локализация Tpr в нуклеопорном комплексе имеет решающее значение для регуляции экспорта мРНК, содержащей интрон, путем прямого или косвенного участия в процессинге и деградации аберрантных транскриптов мРНК.
Образец цитирования: Rajanala K, Nandicoori VK (2012) Локализация нуклеопоринового Tpr в комплексе ядерных пор необходима для опосредованной Tpr регуляции экспорта несплайсированной РНК. ПЛОС ОДИН 7(1): е29921. https://doi.org/10.1371/journal.pone.0029921
Редактор: Хуан Мата, Кембриджский университет, Великобритания
Получено: 6 сентября 2011 г.; Принято: 6 декабря 2011 г.; Опубликовано: 13 января 2012 г.
Авторские права: © 2012 Rajanala, Nandicoori. Это статья с открытым доступом, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Это статья с открытым доступом, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Финансирование: Эта работа поддерживается внутренним и внешним финансированием, предоставленным Департаментом биотехнологии Индии VKN. Спонсоры не участвовали в разработке исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили об отсутствии конкурирующих интересов.
Введение
Нуклеопорин Tpr первоначально был идентифицирован как онкогенный активатор протоонкогенов met, raf и trk [1], [2], [3]. Tpr представляет собой большой белок массой 270 кДа с двухкомпонентной структурой, состоящей из ~1600 остатков α-спирали, спирально-скрученной N-концевой области и высококислотного нескрученного карбокси-конца из ~800 аминокислот [4]. Показано, что клеточные трансформации и опухоли человека происходят за счет слияния N-концевых остатков Tpr (остатки 140–230) с протеинкиназными доменами протоонкогенов met, raf и trk [1], [2], [ 3].Было показано, что Tpr локализован исключительно во внутриядерных филаментах, связанных с нуклеоплазматической стороной NPC, путем прямого связывания с Nup153 [5], [6], [7]. Было показано, что разные виды Metazoan содержат только один ортолог Tpr, тогда как два гомолога, Mlp1 и Mlp2, присутствуют в Saccharomyces cerevisiae и Schizosaccharomyces pombe [8], [9], [10].
Показано, что клеточные трансформации и опухоли человека происходят за счет слияния N-концевых остатков Tpr (остатки 140–230) с протеинкиназными доменами протоонкогенов met, raf и trk [1], [2], [ 3].Было показано, что Tpr локализован исключительно во внутриядерных филаментах, связанных с нуклеоплазматической стороной NPC, путем прямого связывания с Nup153 [5], [6], [7]. Было показано, что разные виды Metazoan содержат только один ортолог Tpr, тогда как два гомолога, Mlp1 и Mlp2, присутствуют в Saccharomyces cerevisiae и Schizosaccharomyces pombe [8], [9], [10].
Функции Tpr включают роли во внутриядерном и ядерно-цитоплазматическом транспорте и в качестве каркасного элемента в ядерной фазе NPC [11], [12], [13], [14].Было показано, что Tpr играет роль в ядерном экспорте белков, содержащих богатый лейцином сигнал ядерного экспорта (NES), а также способствует экспорту белков без явного NES, как в белке Хантингтона [12], [15]. Было показано, что ассоциация белков Mad1 и Mad2 с Tpr влияет на передачу сигналов контрольных точек митотического веретена [16]. Истощение Tpr вызывает фенотип отставания хромосом, и это явление связано с потерей взаимодействия между Tpr и динеиновым комплексом [17]. Гомолог Tpr арабидопсиса участвует в регуляции экспорта мРНК и гомеостаза SUMO, и было показано, что он влияет на различные аспекты развития растений, такие как время цветения [18], [19].Было показано, что взаимодействие между транскрипционным фактором HSF-1 и Tpr способствует экспорту стресс-индуцированной мРНК Hsp-70 [20]. В предыдущем исследовании мы идентифицировали Tpr как субстрат MAP-киназы ERK2 и идентифицировали ERK2-опосредованные сайты фосфорилирования на Tpr [21], [22]. Было продемонстрировано, что Tpr действует как каркас ERK2 в NPC, что, в свою очередь, приводит к фосфорилированию субстратов, которые взаимодействуют с Tpr.
Истощение Tpr вызывает фенотип отставания хромосом, и это явление связано с потерей взаимодействия между Tpr и динеиновым комплексом [17]. Гомолог Tpr арабидопсиса участвует в регуляции экспорта мРНК и гомеостаза SUMO, и было показано, что он влияет на различные аспекты развития растений, такие как время цветения [18], [19].Было показано, что взаимодействие между транскрипционным фактором HSF-1 и Tpr способствует экспорту стресс-индуцированной мРНК Hsp-70 [20]. В предыдущем исследовании мы идентифицировали Tpr как субстрат MAP-киназы ERK2 и идентифицировали ERK2-опосредованные сайты фосфорилирования на Tpr [21], [22]. Было продемонстрировано, что Tpr действует как каркас ERK2 в NPC, что, в свою очередь, приводит к фосфорилированию субстратов, которые взаимодействуют с Tpr.
Традиционно у эукариот несплайсированная РНК сохраняется в ядре, и только процессированная мРНК экспортируется через NPC.Однако ретровирусы разработали механизмы для преодоления этой регуляции, что позволяет экспортировать и, наконец, упаковывать несплайсированную геномную РНК. Эти механизмы можно разделить на два типа: зависимые от Rev и независимые от Rev. Зависимый от Rev путь, используемый вирусом иммунодефицита человека (ВИЧ), использует ретровирусный белок Rev, связанный с элементом ответа Rev (RRE) [3], присутствующим в несплайсированных транскриптах [23], [24]. После связывания с RRE Rev рекрутирует клеточные факторы хозяина, такие как Exportin-1 [25] и Sam68 (Src, связанный с митозом 68), для осуществления ядерного экспорта через NPC.Sam68, член семейства белков STAR (Signal Transduction and Activation of RNA), функционально регулируется ядерными киназами SIK/BRK [26]. Независимый от Rev механизм экспорта несплайсированной РНК используется в вирусе обезьян Mason Pfizer (MMPV). Это опосредовано -цис--действующим элементом, присутствующим в несплайсированном транскрипте, известным как конститутивный транспортный элемент (CTE) [27], который напрямую рекрутирует клеточные факторы хозяина для экспорта интрон-содержащей РНК.
Эти механизмы можно разделить на два типа: зависимые от Rev и независимые от Rev. Зависимый от Rev путь, используемый вирусом иммунодефицита человека (ВИЧ), использует ретровирусный белок Rev, связанный с элементом ответа Rev (RRE) [3], присутствующим в несплайсированных транскриптах [23], [24]. После связывания с RRE Rev рекрутирует клеточные факторы хозяина, такие как Exportin-1 [25] и Sam68 (Src, связанный с митозом 68), для осуществления ядерного экспорта через NPC.Sam68, член семейства белков STAR (Signal Transduction and Activation of RNA), функционально регулируется ядерными киназами SIK/BRK [26]. Независимый от Rev механизм экспорта несплайсированной РНК используется в вирусе обезьян Mason Pfizer (MMPV). Это опосредовано -цис--действующим элементом, присутствующим в несплайсированном транскрипте, известным как конститутивный транспортный элемент (CTE) [27], который напрямую рекрутирует клеточные факторы хозяина для экспорта интрон-содержащей РНК.
В настоящем исследовании мы сообщаем о результатах комплексного анализа роли нуклеопорина Tpr в модулировании импорта/экспорта белка, экспорта мРНК и экспорта несплайсированной РНК. Мы обнаружили, что Tpr, по-видимому, не играет существенной роли в регуляции импорта/экспорта белка и экспорта мРНК. Однако он играет определяющую роль в модуляции CTE-опосредованного экспорта интрон-содержащей РНК. Истощение Tpr приводит к усилению функции CTE, что обеспечивает увеличение экспорта Gag/Pol-CTE РНК, что приводит к последующему пропорциональному увеличению уровней белка Gag/Pol. Наши данные показывают, что Tpr является новым модулятором экспорта несплайсированной РНК в клетках млекопитающих, и его функция не зависит от тех белков, которые, как известно, способствуют CTE-опосредованному экспорту несплайсированной РНК.Результаты нашего исследования четко устанавливают важность локализации Tpr в NPC для облегчения регуляции экспорта несплайсированной РНК в клетках млекопитающих.
Мы обнаружили, что Tpr, по-видимому, не играет существенной роли в регуляции импорта/экспорта белка и экспорта мРНК. Однако он играет определяющую роль в модуляции CTE-опосредованного экспорта интрон-содержащей РНК. Истощение Tpr приводит к усилению функции CTE, что обеспечивает увеличение экспорта Gag/Pol-CTE РНК, что приводит к последующему пропорциональному увеличению уровней белка Gag/Pol. Наши данные показывают, что Tpr является новым модулятором экспорта несплайсированной РНК в клетках млекопитающих, и его функция не зависит от тех белков, которые, как известно, способствуют CTE-опосредованному экспорту несплайсированной РНК.Результаты нашего исследования четко устанавливают важность локализации Tpr в NPC для облегчения регуляции экспорта несплайсированной РНК в клетках млекопитающих.
Результаты
Tpr не играет значительной роли в транспорте клеточных белков или в экспорте мРНК
Сообщалось, что нуклеопориновый Tpr играет роль в ядерном экспорте белков, содержащих сигнал ядерного экспорта, богатый лейцином, [12] и также сообщалось, что эктопическая экспрессия Tpr млекопитающих приводит к накоплению поли (A) + РНК в ядре [28]. Мы стремились всесторонне исследовать роль Tpr в ядерно-цитоплазматическом транспорте макромолекул. Чтобы изучить функцию Tpr в клеточном транспорте белков и ядерном экспорте мРНК, мы истощили белок Tpr в клетках HEK293T, используя три независимых олигонуклеотида siRNA. Когда уровни Tpr анализировали через 48 часов после трансфекции, снижение уровней Tpr можно было увидеть для всех трех олигонуклеотидов siRNA (фиг. 1A). Непрямая иммунофлуоресцентная микроскопия с использованием мышиных моноклональных антител против Tpr подтвердила эти данные (рис.1Б).
Мы стремились всесторонне исследовать роль Tpr в ядерно-цитоплазматическом транспорте макромолекул. Чтобы изучить функцию Tpr в клеточном транспорте белков и ядерном экспорте мРНК, мы истощили белок Tpr в клетках HEK293T, используя три независимых олигонуклеотида siRNA. Когда уровни Tpr анализировали через 48 часов после трансфекции, снижение уровней Tpr можно было увидеть для всех трех олигонуклеотидов siRNA (фиг. 1A). Непрямая иммунофлуоресцентная микроскопия с использованием мышиных моноклональных антител против Tpr подтвердила эти данные (рис.1Б).
Рис. 1. Нокдаун Tpr в клетках HEK293T, опосредованный РНК-интерференцией.
(A) Вестерн-блот-анализ экстрактов цельных клеток, полученных из клеток через 48 часов после обработки либо неспецифической миРНК (NS-Si), либо тремя различными миРНК Tpr (TSi, TSi-1, TSi-2), зондированных с помощью анти-Tpr и анти-ERK-антитела. (B) Иммунофлуоресцентный анализ клеток через 48 часов после трансфекции различными олигонуклеотидами миРНК Tpr. Четкое окрашивание ядерной мембраны наблюдается в клетках, обработанных NS-Si, тогда как в клетках, где Tpr нокдаун, обнаруживаются только следы окрашивания.
Четкое окрашивание ядерной мембраны наблюдается в клетках, обработанных NS-Si, тогда как в клетках, где Tpr нокдаун, обнаруживаются только следы окрашивания.
https://doi.org/10.1371/journal.pone.0029921.g001
Love и др. [29] создали чрезвычайно полезную систему для исследования импорта и экспорта белков в клетках HeLa. В этих клетках химерный белок Rev- Glucocorticoid-GFP Receptor (химерный GFP) локализуется в цитозоле в отсутствие какой-либо обработки, а при добавлении дексаметазона транслоцируется в ядро. После удаления дексаметазона химерный GFP экспортируется обратно в цитоплазму.Клетки, экспрессирующие этот химерный белок GFP, трансфицировали олигонуклеотидами либо неспецифической siRNA (NS-Si), либо Tpr-siRNA (TSi) и инкубировали в течение 48 часов для достижения нокдауна белка Tpr (фиг. 2A). Когда импорт химерного белка GFP исследовали путем инкубации клеток с дексаметазоном, скорость импорта была одинаковой для клеток, обработанных NS-Si и TSi (рис. 2B), что указывает на отсутствие какой-либо роли Tpr в импорте белка. В дальнейшем визуализировали экспорт химерного GFP-белка через различные промежутки времени после удаления дексаметазона.Интересно, что мы наблюдали небольшое, но воспроизводимое снижение скорости экспорта химерного белка GFP в клетках, обработанных TSi, по сравнению с клетками, обработанными NS-Si, через 30 и 60 мин после смывания препарата/гормона. Однако через 2 ч после удаления препарата в обоих случаях отмечена полная транслокация химерного GFP в цитозоль (рис. 2В). Эти результаты показывают, что Tpr может играть ограниченную роль в модуляции скорости экспорта белка. Чтобы исследовать роль Tpr в экспорте процессированных поли (A) + мРНК, мы сбили экспрессию Tpr (рис.2D) и выполнили флуоресцентную гибридизацию in situ с использованием меченого FITC олиго(dT) зонда (рис. 2E). Распределение мРНК поли(А) + оказалось сопоставимым как в контроле, так и в клетках, лишенных Tpr (рис. 2Д). На основании этих результатов мы делаем вывод, что Tpr не играет роли в транслокации белков или мРНК поли(А) + через ядерную мембрану.
2B), что указывает на отсутствие какой-либо роли Tpr в импорте белка. В дальнейшем визуализировали экспорт химерного GFP-белка через различные промежутки времени после удаления дексаметазона.Интересно, что мы наблюдали небольшое, но воспроизводимое снижение скорости экспорта химерного белка GFP в клетках, обработанных TSi, по сравнению с клетками, обработанными NS-Si, через 30 и 60 мин после смывания препарата/гормона. Однако через 2 ч после удаления препарата в обоих случаях отмечена полная транслокация химерного GFP в цитозоль (рис. 2В). Эти результаты показывают, что Tpr может играть ограниченную роль в модуляции скорости экспорта белка. Чтобы исследовать роль Tpr в экспорте процессированных поли (A) + мРНК, мы сбили экспрессию Tpr (рис.2D) и выполнили флуоресцентную гибридизацию in situ с использованием меченого FITC олиго(dT) зонда (рис. 2E). Распределение мРНК поли(А) + оказалось сопоставимым как в контроле, так и в клетках, лишенных Tpr (рис. 2Д). На основании этих результатов мы делаем вывод, что Tpr не играет роли в транслокации белков или мРНК поли(А) + через ядерную мембрану.
Рис. 2. Истощение Tpr не оказывает существенного влияния на транспорт клеточных белков и экспорт мРНК.
(A) Вестерн-блоттинг экстрактов клеток HeLa, сделанный через 48 часов после обработки TSi.(B) Клетки HeLa, которые стабильно экспрессируют репортерную конструкцию GFP, чувствительную к гормонам (RGG), трансфицировали NS-Si или TSi. Импорт химерного GFP контролировали путем фиксации клеток 4% параформальдегидом в разное время после обработки дексаметазоном. (C) Экспорт конструкции RGG отслеживали в указанные моменты времени после удаления гормона. (D) Вестерн-блоттинг, изображающий нокдаун Tpr в клетках HEK293T через 48 часов после трансфекции миРНК. (E) Флуоресцентная гибридизация in situ с зондом FITC-oligo(dT) для оценки распределения поли(A) + мРНК в клетках HEK293T, трансфицированных TSi.
https://doi.org/10.1371/journal.pone.0029921.g002
Tpr модулирует CTE-зависимый экспорт несплайсированной РНК
Сообщалось, что гомологи Tpr в S. cerevisiae , Mlp1 и Mlp2, играют роль в экспорте несплайсированной РНК [30]. Для анализа роли Tpr в ядерно-цитоплазматическом экспорте интрон-содержащей РНК мы использовали хорошо охарактеризованные репортерные конструкции Gag/Pol, содержащие либо Rev-ответный элемент (RRE) [3], либо конститутивный транспортный элемент (CTE) [26]. 31], [32], [33], [34].Эти репортерные конструкции содержат кодирующие последовательности белков Gag/Pol ВИЧ внутри интрона, за которыми следует либо RRE, либо CTE. Сначала мы рассмотрели возможность роли Tpr в экспорте, зависящем от RRE. Вестерн-блоттинг показал, что, когда Tpr действительно был нокдаун, наблюдалась незначительная вариация продуктов расщепления белка Gag р55, р41 и р24 (фиг. 3А). Уровни белка Gag в цитоплазме количественно определяли с помощью р24 ELISA, который измеряет количество обработанного белка Gag (р24).Из представленных данных видно (рис. 3B, рис. S1A и S1B), что уровни p24 в экстрактах оставались одинаковыми, независимо от уровней белка Tpr, что указывает на то, что Tpr не играет никакой роли в зависимых от RRE-Rev экспорт несплайсированной РНК.
cerevisiae , Mlp1 и Mlp2, играют роль в экспорте несплайсированной РНК [30]. Для анализа роли Tpr в ядерно-цитоплазматическом экспорте интрон-содержащей РНК мы использовали хорошо охарактеризованные репортерные конструкции Gag/Pol, содержащие либо Rev-ответный элемент (RRE) [3], либо конститутивный транспортный элемент (CTE) [26]. 31], [32], [33], [34].Эти репортерные конструкции содержат кодирующие последовательности белков Gag/Pol ВИЧ внутри интрона, за которыми следует либо RRE, либо CTE. Сначала мы рассмотрели возможность роли Tpr в экспорте, зависящем от RRE. Вестерн-блоттинг показал, что, когда Tpr действительно был нокдаун, наблюдалась незначительная вариация продуктов расщепления белка Gag р55, р41 и р24 (фиг. 3А). Уровни белка Gag в цитоплазме количественно определяли с помощью р24 ELISA, который измеряет количество обработанного белка Gag (р24).Из представленных данных видно (рис. 3B, рис. S1A и S1B), что уровни p24 в экстрактах оставались одинаковыми, независимо от уровней белка Tpr, что указывает на то, что Tpr не играет никакой роли в зависимых от RRE-Rev экспорт несплайсированной РНК.
Рисунок 3. Повышенные уровни p24 в результате усиленной функции CTE наблюдаются в клетках с нокдауном Tpr.
(A) Клетки HEK293T трансфицировали либо NS-Si, либо различными олигонуклеотидами siRNA против Tpr вместе со 100 нг Gag/PR-RRE, 75 нг pcDNA3-Flag-Rev и 100 нг конструкций CMV-β-Gal .Через 48 часов после трансфекции лизаты разделяли на SDS-PAGE, переносили на нитроцеллюлозную мембрану и исследовали антителами против Tpr, ERK и p24. (B) анализировали уровни p24 и β-галактозидазы в каждом из образцов. Затем значения p24 были скорректированы с учетом изменений показаний β-Gal, и здесь представлены нормализованные значения. Представлены средние значения трех независимых трансфекций; планки погрешностей представляют собой стандартное отклонение. (C) Вестерн-блот экстрактов клеток HEK293T, демонстрирующий повышенные уровни продуктов расщепления белка Gag/pol в клетках, трансфицированных репортерной конструкцией Gag/Pol-CTE, CMV-β-Gal и различными миРНК Tpr.(D) Эффект нокдауна Tpr на экспрессию p24 из репортера Gag/pol-CTE, что продемонстрировано показаниями p24 ELISA после нормализации по уровням β-галактозидазы.
https://doi.org/10.1371/journal.pone.0029921.g003
Затем мы исследовали возможную роль Tpr в регуляции CTE-зависимого экспорта несплайсированной РНК. Вестерн-блот-анализ экстрактов, полученных из клеток, обработанных миРНК Tpr, показал, что снижение экспрессии Tpr значительно увеличивает уровни продуктов расщепления белка Gag p55, p41 и p24 (фиг.3С). Мы наблюдали примерно 8–10-кратное увеличение нормализованного уровня p24 в экстрактах, приготовленных из клеток, трансфицированных TSi, по сравнению с клетками, трансфицированными NS-Si (рис. 3D, рис. S1C и S1D). Затем мы стремились исследовать, можно ли наблюдать феномен опосредованной Tpr регуляции экспорта несплайсированной РНК в клетках, отличных от HEK293T. Результаты продемонстрировали усиленную функцию CTE при истощении Tpr в клеточных линиях COS-1 и HeLa (рис. 4A и 4B, рис. S2A и S2B). Хотя кратное увеличение экспорта несплайсированной РНК различно для разных клеточных линий, ключевое открытие, заключающееся в том, что Tpr играет роль в удержании несплайсированной РНК в ядре, может последовательно наблюдаться во всех трех клеточных линиях. Чтобы исключить возможность того, что обнаруженное увеличение ядерного экспорта репортерного гена ограничено геном gag/pol , мы создали репортерную конструкцию люциферазы (Luc), в которую была вставлена кодирующая последовательность гена luc . между 5′- и 3′-последовательностями сайта сплайсинга, происходящими из гена gag/pol ВИЧ , с последующим CTE (фиг. 4C). Как видно из рисунка 4, снижение уровня Tpr (рис. 4D) приводило к увеличению нормализованной активности люциферазы примерно в 6–8 раз (рис.4E, фиг. S2C и S2D). Взятые вместе, эти результаты указывают на регуляторную роль Tpr в модуляции CTE-зависимого экспорта несплайсированной РНК.
Чтобы исключить возможность того, что обнаруженное увеличение ядерного экспорта репортерного гена ограничено геном gag/pol , мы создали репортерную конструкцию люциферазы (Luc), в которую была вставлена кодирующая последовательность гена luc . между 5′- и 3′-последовательностями сайта сплайсинга, происходящими из гена gag/pol ВИЧ , с последующим CTE (фиг. 4C). Как видно из рисунка 4, снижение уровня Tpr (рис. 4D) приводило к увеличению нормализованной активности люциферазы примерно в 6–8 раз (рис.4E, фиг. S2C и S2D). Взятые вместе, эти результаты указывают на регуляторную роль Tpr в модуляции CTE-зависимого экспорта несплайсированной РНК.
Рисунок 4. Истощение Tpr млекопитающих значительно усиливает функцию CTE.
(A) Клетки HEK293T, COS-1 и HeLa трансфицировали либо NS-Si, либо TSi вместе с репортерной конструкцией Gag/Pol-CTE, и лизаты исследовали антителами против Tpr, против ERK. (B) Лизаты клеток анализировали на экспрессию p24 и β-Gal, и уровни p24 нормализовали с использованием показаний β-Gal. (C) Схематическое изображение репортерной конструкции люциферазы-CTE (Luc-CTE). (D) Вестерн-блот-анализ экстрактов клеток HEK293T, совместно трансфицированных NS-Si или TSi, CTE-Luc и CMV-β-Gal, для изучения нокдауна Tpr через 48 часов после трансфекции. (E) Активность люциферазы в образцах была зарегистрирована, и показания были скорректированы с учетом изменений показаний β-Gal.
(C) Схематическое изображение репортерной конструкции люциферазы-CTE (Luc-CTE). (D) Вестерн-блот-анализ экстрактов клеток HEK293T, совместно трансфицированных NS-Si или TSi, CTE-Luc и CMV-β-Gal, для изучения нокдауна Tpr через 48 часов после трансфекции. (E) Активность люциферазы в образцах была зарегистрирована, и показания были скорректированы с учетом изменений показаний β-Gal.
https://doi.org/10.1371/journal.pone.0029921.g004
Эктопическая и стабильная экспрессия Tpr, устойчивого к siRNA, восстанавливает CTE-опосредованный экспорт несплайсированной РНК
Чтобы подтвердить наши результаты, мы попытались восстановить фенотип повышенного экспорта несплайсированной РНК путем совместной трансфекции клеток плазмидой, содержащей ген tpr , устойчивый к миРНК, и олигонуклеотид TSi.Чтобы создать клон Tpr, устойчивый к siRNA, мы ввели молчащие точечные мутации в позиции колебания в последовательности-мишени TSi путем перекрывающейся ПЦР (фиг. 5A). Как и ожидалось, в клетках, совместно трансфицированных TSi и конструкцией FLAG-Tpr, обнаруженные уровни Tpr аналогичны уровням, наблюдаемым в клетках, трансфицированных TSi (фиг. 5B; сравните дорожку 4 с 2). Однако при совместной трансфекции клеток конструкцией TSi и FLAG-Tpr-Si обнаруженные уровни Tpr были почти эквивалентны контролю (рис.5Б; сравните дорожку 6 с 1), что указывает на то, что спасательная плазмида действительно устойчива к миРНК. Непрямая иммунофлуоресцентная микроскопия с использованием мышиных моноклональных анти-Flag антител показала, что эффективность трансфекции составляет примерно 40–60% (рис. 5C и рис. S3A и S6C). Подобно результатам на рисунке 3, мы наблюдали значительное увеличение уровней нормализованного p24, когда внутриклеточный Tpr был нокдаун с использованием TSi, который предсказуемо не изменился, когда клетки были котрансфецированы с помощью FLAG-Tpr (рис.5D, фиг. S3B и S3C). Мы наблюдали почти трехкратное снижение уровней p24, когда уровни Tpr восстанавливались путем котрансфекции клеток конструкцией, устойчивой к siRNA.
5A). Как и ожидалось, в клетках, совместно трансфицированных TSi и конструкцией FLAG-Tpr, обнаруженные уровни Tpr аналогичны уровням, наблюдаемым в клетках, трансфицированных TSi (фиг. 5B; сравните дорожку 4 с 2). Однако при совместной трансфекции клеток конструкцией TSi и FLAG-Tpr-Si обнаруженные уровни Tpr были почти эквивалентны контролю (рис.5Б; сравните дорожку 6 с 1), что указывает на то, что спасательная плазмида действительно устойчива к миРНК. Непрямая иммунофлуоресцентная микроскопия с использованием мышиных моноклональных анти-Flag антител показала, что эффективность трансфекции составляет примерно 40–60% (рис. 5C и рис. S3A и S6C). Подобно результатам на рисунке 3, мы наблюдали значительное увеличение уровней нормализованного p24, когда внутриклеточный Tpr был нокдаун с использованием TSi, который предсказуемо не изменился, когда клетки были котрансфецированы с помощью FLAG-Tpr (рис.5D, фиг. S3B и S3C). Мы наблюдали почти трехкратное снижение уровней p24, когда уровни Tpr восстанавливались путем котрансфекции клеток конструкцией, устойчивой к siRNA. Однако даже при повторном эксперименте уровни нормализованного р24 не снижались до контрольных значений. Скорее всего, это связано с тем, что все клетки с нокдауном Tpr не экспрессируют FLAG-Tpr-Si, а уровни экспрессии варьируют от клетки к клетке (рис. 5С). Чтобы решить эту проблему, мы создали стабильные клеточные линии HEK293T, экспрессирующие либо FLAG-Tpr дикого типа, либо FLAG-Tpr-Si.Данные непрямой иммунофлуоресценции предполагают аналогичную и однородную экспрессию конструкций FLAG-Tpr и FLAG-Tpr-Si (фиг. 5E). Важно отметить, что когда лизаты исследовали с помощью FLAG-антител, мы наблюдали, что уровни экспрессии FLAG-меченого Tpr в стабильно трансфицированных клетках были почти эквивалентными (фиг. 5F). Нормализованные уровни p24, полученные в результате истощения Tpr в стабильной клеточной линии Flag-Tpr, были аналогичны уровням, полученным с родительскими клетками 293T (фиг. 5G). Когда стабильные клетки Flag-Tpr-Si трансфицировали либо NS-Si, либо TSi и Gag/Pol-CTE, мы наблюдали почти четырехкратное снижение уровней p24 по сравнению со стабильной клеточной линией FLAG-Tpr (рис.
Однако даже при повторном эксперименте уровни нормализованного р24 не снижались до контрольных значений. Скорее всего, это связано с тем, что все клетки с нокдауном Tpr не экспрессируют FLAG-Tpr-Si, а уровни экспрессии варьируют от клетки к клетке (рис. 5С). Чтобы решить эту проблему, мы создали стабильные клеточные линии HEK293T, экспрессирующие либо FLAG-Tpr дикого типа, либо FLAG-Tpr-Si.Данные непрямой иммунофлуоресценции предполагают аналогичную и однородную экспрессию конструкций FLAG-Tpr и FLAG-Tpr-Si (фиг. 5E). Важно отметить, что когда лизаты исследовали с помощью FLAG-антител, мы наблюдали, что уровни экспрессии FLAG-меченого Tpr в стабильно трансфицированных клетках были почти эквивалентными (фиг. 5F). Нормализованные уровни p24, полученные в результате истощения Tpr в стабильной клеточной линии Flag-Tpr, были аналогичны уровням, полученным с родительскими клетками 293T (фиг. 5G). Когда стабильные клетки Flag-Tpr-Si трансфицировали либо NS-Si, либо TSi и Gag/Pol-CTE, мы наблюдали почти четырехкратное снижение уровней p24 по сравнению со стабильной клеточной линией FLAG-Tpr (рис. 5G и рис. S3D и S3E). Эти результаты показывают, что регуляция опосредованной CTE экспрессии гена p24 может быть специфически связана с изменениями уровней Tpr в клетках HEK293T.
5G и рис. S3D и S3E). Эти результаты показывают, что регуляция опосредованной CTE экспрессии гена p24 может быть специфически связана с изменениями уровней Tpr в клетках HEK293T.
Рис. 5. Эктопическая и стабильная экспрессия Tpr, устойчивого к siRNA, восстанавливает CTE-опосредованный экспорт несплайсированной РНК.
(A) Схематическое изображение мутаций точки молчания, которые были введены в нуклеотидную последовательность Tpr, чтобы защитить ее от нацеливания на дуплексы siRNA. (B) Иммуноблот, демонстрирующий восстановление уровней Tpr при совместной трансфекции конструкции FLAG-Tpr-Si с TSi.Для трансфекции использовали 2 мкг Flag-Tpr или Flag-Tpr-Si. (C) Непрямая иммунофлуоресцентная микроскопия клеток HEK293T, трансфицированных клоном Flag-Tpr дикого типа или клоном Tpr, устойчивым к миРНК, вместе с NS-Si или TSi с использованием мышиных моноклональных антител против Flag (D) p24 и уровни β-галактозидазы в каждом из образцы были проанализированы. Затем значения p24 корректировали с учетом изменений показаний β-Gal. (E) Клетки HEK293T, стабильно экспрессирующие Flag-Tpr или Flag-Tpr-Si, трансфицировали либо NS-Si, либо TSi вместе с плазмидами Gag/Pol-CTE и CMV-β-Gal.Вестерн-блоттинг экстрактов цельных клеток, зондированных антителами против Tpr, против FLAG и против ERK, демонстрирует стабильную экспрессию. (F) Иммунофлуоресцентный анализ стабильных клеток Flag-Tpr или Flag-Tpr-Si после 2 дней трансфекции олигонуклеотидами NS-Si или TSi. (G) Лизаты клеток анализировали на экспрессию p24 и β-Gal, и уровни p24 нормализовали с помощью показаний β-Gal.
(E) Клетки HEK293T, стабильно экспрессирующие Flag-Tpr или Flag-Tpr-Si, трансфицировали либо NS-Si, либо TSi вместе с плазмидами Gag/Pol-CTE и CMV-β-Gal.Вестерн-блоттинг экстрактов цельных клеток, зондированных антителами против Tpr, против FLAG и против ERK, демонстрирует стабильную экспрессию. (F) Иммунофлуоресцентный анализ стабильных клеток Flag-Tpr или Flag-Tpr-Si после 2 дней трансфекции олигонуклеотидами NS-Si или TSi. (G) Лизаты клеток анализировали на экспрессию p24 и β-Gal, и уровни p24 нормализовали с помощью показаний β-Gal.
https://doi.org/10.1371/journal.pone.0029921.g005
Истощение Tpr усиливает опосредованный CTE экспорт несплайсированной РНК из ядра
Повышение нормализованного уровня р24 также может быть связано с повышенной трансляцией gag/pol РНК в цитозоле.Чтобы установить, действительно ли Tpr-зависимое увеличение уровней белка p24 связано с экспортом несплайсированной РНК, мы провели количественный ПЦР-анализ в реальном времени. Ядерное и цитоплазматическое фракционирование проводили, как описано, и из экстрактов готовили РНК и белковые фракции. Вестерн-блоттинг анализ (фиг. 6А) ясно показал присутствие Tpr в ядерной фракции и тубулина в цитоплазматической фракции. Кроме того, растворимые ядерные белки 53BP1, CyclinA и ядерный маркер Lamin можно было обнаружить только в ядерной фракции, что указывает на то, что полученные фракции не содержали каких-либо загрязнений.ПЦР-анализ в реальном времени установил, что цитоплазматическая несплайсированная РНК Gag/Pol-CTE была значительно выше в клетках, лишенных Tpr, по сравнению с клетками, обработанными NS-Si, что предполагает повышенный экспорт транскриптов несплайсированной РНК (фиг. 6B). Подобное кратное изменение уровней ядерной и цитоплазматической мРНК также наблюдалось в случае несплайсированной РНК Luc-CTE (рис. 6С). Увеличение уровней цитоплазматической несплайсированной РНК отражается в пропорциональном увеличении уровней p24, показанном на рисунках 3, 4 и 5, что подтверждает тот факт, что Tpr регулирует CTE-опосредованный экспорт мРНК, содержащей интрон.
Ядерное и цитоплазматическое фракционирование проводили, как описано, и из экстрактов готовили РНК и белковые фракции. Вестерн-блоттинг анализ (фиг. 6А) ясно показал присутствие Tpr в ядерной фракции и тубулина в цитоплазматической фракции. Кроме того, растворимые ядерные белки 53BP1, CyclinA и ядерный маркер Lamin можно было обнаружить только в ядерной фракции, что указывает на то, что полученные фракции не содержали каких-либо загрязнений.ПЦР-анализ в реальном времени установил, что цитоплазматическая несплайсированная РНК Gag/Pol-CTE была значительно выше в клетках, лишенных Tpr, по сравнению с клетками, обработанными NS-Si, что предполагает повышенный экспорт транскриптов несплайсированной РНК (фиг. 6B). Подобное кратное изменение уровней ядерной и цитоплазматической мРНК также наблюдалось в случае несплайсированной РНК Luc-CTE (рис. 6С). Увеличение уровней цитоплазматической несплайсированной РНК отражается в пропорциональном увеличении уровней p24, показанном на рисунках 3, 4 и 5, что подтверждает тот факт, что Tpr регулирует CTE-опосредованный экспорт мРНК, содержащей интрон. К нашему удивлению, мы обнаружили, что уровни ядерной мРНК CTE также были примерно в 2–3 раза выше в отсутствие Tpr (рис. 6B и 6C). Дрожжевые гомологи Tpr, белки Mlp, как было показано, подавляют экспрессию генов в ответ на присутствие аберрантных транскриптов РНК [35]. Мы предполагаем, что увеличение пулов CTE-мРНК в ядре может быть связано с повышенной экспрессией транскриптов CTE-мРНК в клетках, лишенных Tpr, и/или повышенной стабильностью этих транскриптов в ядре при нокдауне Tpr.Возможно, что помимо регуляции экспорта несплайсированных РНК, заставляя их удерживаться в ядре, Tpr может играть роль в модуляции процессинга молекул мРНК до того, как транскрипты действительно экспортируются.
К нашему удивлению, мы обнаружили, что уровни ядерной мРНК CTE также были примерно в 2–3 раза выше в отсутствие Tpr (рис. 6B и 6C). Дрожжевые гомологи Tpr, белки Mlp, как было показано, подавляют экспрессию генов в ответ на присутствие аберрантных транскриптов РНК [35]. Мы предполагаем, что увеличение пулов CTE-мРНК в ядре может быть связано с повышенной экспрессией транскриптов CTE-мРНК в клетках, лишенных Tpr, и/или повышенной стабильностью этих транскриптов в ядре при нокдауне Tpr.Возможно, что помимо регуляции экспорта несплайсированных РНК, заставляя их удерживаться в ядре, Tpr может играть роль в модуляции процессинга молекул мРНК до того, как транскрипты действительно экспортируются.
Рис. 6. Истощение Tpr усиливает опосредованный CTE экспорт несплайсированной РНК из ядра.
(A) Вестерн-блоттинг цитозольной и ядерной фракций с использованием антител против тубулина, ламина, Tpr, 53BP1 и циклина A. (B) ПЦР-анализ в реальном времени мРНК, выделенной из ядерных и цитоплазматических фракций клеток HEK293T, котрансфицированных конструкцией Gag/Pol-CTE и NS-Si или TSi. (C) Уровни РНК Luc-CTE в ядре и цитоплазме клеток, трансфицированных конструкцией pcDNA3-Luc-CTE и NS-Si или TSi, измеренные с помощью ПЦР в реальном времени.
(C) Уровни РНК Luc-CTE в ядре и цитоплазме клеток, трансфицированных конструкцией pcDNA3-Luc-CTE и NS-Si или TSi, измеренные с помощью ПЦР в реальном времени.
https://doi.org/10.1371/journal.pone.0029921.g006
Опосредованная Tpr регуляция экспорта несплайсированной РНК не зависит от функций Sam68 и Tap
Предыдущие отчеты продемонстрировали критическую роль белков Sam68 и Tap в усилении функции CTE за счет увеличения стабильности и использования несплайсированной РНК [26], [34].Чтобы понять механизм, лежащий в основе опосредованной Tpr регуляции, мы изучили влияние истощения Sam68 и Tap, а также сверхэкспрессии на опосредованный CTE экспорт в клетках с дефицитом Tpr. Клетки HEK293T котрансфицировали репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal вместе с NS-Si или TSi в сочетании либо с Tap-siRNA, либо с Sam68-siRNA, и анализировали через 96 часов после обработки siRNA для получения эффективных нокдауны. Вестерн-блоттинг лизатов показал снижение уровней белков Tpr и Sam68 в ответ на обработку их соответствующими миРНК (фиг. 7А). Однако истощение Tap при обработке siRNA было не очень эффективным (фиг. 7A). Анализ нормализованного p24 в клеточных лизатах показал, что истощение Tap или Sam68 само по себе не сильно влияет на экспорт несплайсированной РНК (фиг. 7B, фиг. S4A и S4B). Интересно, что истощение Tpr и Sam68 вместе приводило к уменьшению p24 в цитозоле. Это может быть связано с тем фактом, что известно, что Sam68 необходим для стабилизации несплайсированной РНК [36], которая может быть до некоторой степени скомпрометирована в его отсутствие.Было показано, что Tap/Nxf1 влияет на экспорт мРНК из ядра в различных модельных системах [37], [38], [39], [40]. Тем не менее, мы не наблюдали заметного снижения при частичном истощении Tap ни уровней p24, ни β-GAL (рис. S4A и S4B). Различия между более ранними исследованиями Tap siRNA и нашими результатами могут быть связаны с различиями в эффективности siRNA в подавлении экспрессии Tap, поскольку нокдаун, обнаруженный в нашем эксперименте, не так эффективен, как представленные в более ранних отчетах.
7А). Однако истощение Tap при обработке siRNA было не очень эффективным (фиг. 7A). Анализ нормализованного p24 в клеточных лизатах показал, что истощение Tap или Sam68 само по себе не сильно влияет на экспорт несплайсированной РНК (фиг. 7B, фиг. S4A и S4B). Интересно, что истощение Tpr и Sam68 вместе приводило к уменьшению p24 в цитозоле. Это может быть связано с тем фактом, что известно, что Sam68 необходим для стабилизации несплайсированной РНК [36], которая может быть до некоторой степени скомпрометирована в его отсутствие.Было показано, что Tap/Nxf1 влияет на экспорт мРНК из ядра в различных модельных системах [37], [38], [39], [40]. Тем не менее, мы не наблюдали заметного снижения при частичном истощении Tap ни уровней p24, ни β-GAL (рис. S4A и S4B). Различия между более ранними исследованиями Tap siRNA и нашими результатами могут быть связаны с различиями в эффективности siRNA в подавлении экспрессии Tap, поскольку нокдаун, обнаруженный в нашем эксперименте, не так эффективен, как представленные в более ранних отчетах. Чтобы решить эту проблему, мы повторили эксперимент, включив две дополнительные миРНК, одну альтернативную миРНК (Tap-siRNA-2) и вторую, пул из четырех разных siРНК (Tap-siRNA-SP), чтобы истощить Tap/Nxf1. белок. Хотя нокдаун, полученный с помощью Tap-siRNA, был подобен нашему более раннему наблюдению, как Tap-siRNA-2, так и Tap-siRNA-SP были весьма эффективны в истощении белка Tap (Fig. 7C). Мы также наблюдали, что восстановление клеток было ниже после обработки более новыми миРНК по сравнению с клетками, трансфицированными Тап-миРНК.В соответствии с предыдущими исследованиями, когда мы истощали Tap с помощью siRNA2 и siRNA-SP, мы наблюдали значительное снижение активности β-галактозидазы в лизатах (~ 50%; рис. 7E). Поскольку на активность β-галактозидазы влияло истощение TAP, мы не нормализовали показания p24. Интересно, что мы не обнаружили существенного снижения уровней р24, что указывает на то, что экспорт несплайсированной РНК, по-видимому, не зависит от истощения ТАР (рис. 7D).
Чтобы решить эту проблему, мы повторили эксперимент, включив две дополнительные миРНК, одну альтернативную миРНК (Tap-siRNA-2) и вторую, пул из четырех разных siРНК (Tap-siRNA-SP), чтобы истощить Tap/Nxf1. белок. Хотя нокдаун, полученный с помощью Tap-siRNA, был подобен нашему более раннему наблюдению, как Tap-siRNA-2, так и Tap-siRNA-SP были весьма эффективны в истощении белка Tap (Fig. 7C). Мы также наблюдали, что восстановление клеток было ниже после обработки более новыми миРНК по сравнению с клетками, трансфицированными Тап-миРНК.В соответствии с предыдущими исследованиями, когда мы истощали Tap с помощью siRNA2 и siRNA-SP, мы наблюдали значительное снижение активности β-галактозидазы в лизатах (~ 50%; рис. 7E). Поскольку на активность β-галактозидазы влияло истощение TAP, мы не нормализовали показания p24. Интересно, что мы не обнаружили существенного снижения уровней р24, что указывает на то, что экспорт несплайсированной РНК, по-видимому, не зависит от истощения ТАР (рис. 7D).
Рисунок 7. Опосредованная Tpr регуляция экспорта несплайсированной РНК не зависит от функций Tap/Nxf1 и Sam68.
Опосредованная Tpr регуляция экспорта несплайсированной РНК не зависит от функций Tap/Nxf1 и Sam68.
(A) Клетки трансфицировали 1 мкг миРНК против Sam68 или Tap/Nxf1 вместе с NS-Si или TSi. Клетки повторно высевали на следующий день и через 24 часа после повторного посева клетки еще раз трансфицировали олигонуклеотидами siRNA и репортерными конструкциями. Вестерн-блот-анализ экстрактов трансфицированных клеток HEK293T, подтверждающий истощение белков Tpr, Sam68 и Tap/Nxf1 при обработке соответствующими миРНК. (B) Через 48 часов после второй трансфекции оценивали степень экспрессии репортерного гена из трансфицированных конструкций Gag/Pol-CTE и CMV-β-Gal.Показания p24 ELISA, полученные из образцов, были скорректированы с учетом вариаций показаний β-галактозидазы. (C) Клетки трансфицировали 1 мкг различных олигонуклеотидов siRNA против Tap/Nxf1 вместе с NS-Si или TSi. Клетки повторно высевали на следующий день и через 24 часа после повторного посева клетки еще раз трансфицировали олигонуклеотидами siRNA и репортерными конструкциями. Вестерн-блоттинг экстрактов трансфицированных клеток HEK293T для анализа истощения белков Tpr и Tap/Nxf1. (D и E) Оценивали степень экспрессии репортерного гена из трансфицированных конструкций Gag/Pol-CTE и CMV-β-Gal.
Вестерн-блоттинг экстрактов трансфицированных клеток HEK293T для анализа истощения белков Tpr и Tap/Nxf1. (D и E) Оценивали степень экспрессии репортерного гена из трансфицированных конструкций Gag/Pol-CTE и CMV-β-Gal.
https://doi.org/10.1371/journal.pone.0029921.g007
Было показано, что сверхэкспрессия Sam68 повышает стабильность и использование несплайсированной РНК, что приводит к повышению уровня p24 [26]. Было показано, что сверхэкспрессия tap улучшает цитоплазматическое использование мРНК Gag/Pol-CTE [34]. Если бы истощение Tpr и сверхэкспрессия Sam68 усиливали экспорт взаимозависимым образом, комбинаторный эффект истощения и сверхэкспрессии был бы не больше, чем независимые эффекты.Однако, если бы они модулировали процесс независимо, можно было бы ожидать кумулятивного эффекта. Чтобы рассмотреть эти две возможности, мы сверхэкспрессировали либо HA-Sam68, либо HA-Tap в клетках, трансфицированных либо NS-Si, либо TSi, и измерили нормализованные уровни p24 в экстрактах. Данные вестерн-блоттинга, представленные на фигуре 8А, показывают эффективное истощение Tpr и сверхэкспрессию HA-Tap и HA-Sam68. В образцах, где Tap или Sam68 были сверхэкспрессированы в присутствии NS-Si, мы обнаружили увеличение нормализованного p24 в экстрактах по сравнению только с NS-Si (рис.8Б). Истощение Tpr само по себе оказывало значительное влияние на уровни p24 в экстракте (фиг. 8B). Интересно, что в образце, где Tap был сверхэкспрессирован в присутствии TSi, мы не наблюдали дальнейшего увеличения (рис. 8B, рис. S4C и S4D). Напротив, когда Sam68 сверхэкспрессировался в клетках с истощением Tpr, мы наблюдали умеренное синергетическое увеличение p24. Кроме того, анализ уровней РНК Gag/Pol-CTE в этих образцах с помощью количественной ПЦР в реальном времени продемонстрировал ту же тенденцию (фиг. 8C). Истощение Tpr само по себе увеличивало уровни РНК Gag/Pol как в ядре, так и в цитоплазме, которые существенно не менялись при сверхэкспрессии Tap (рис.8С). Это не очень удивительно, так как показано, что Tap улучшает цитоплазматическую утилизацию Gag/Pol-CTE РНК, что может происходить только после ее экспорта [34].
Данные вестерн-блоттинга, представленные на фигуре 8А, показывают эффективное истощение Tpr и сверхэкспрессию HA-Tap и HA-Sam68. В образцах, где Tap или Sam68 были сверхэкспрессированы в присутствии NS-Si, мы обнаружили увеличение нормализованного p24 в экстрактах по сравнению только с NS-Si (рис.8Б). Истощение Tpr само по себе оказывало значительное влияние на уровни p24 в экстракте (фиг. 8B). Интересно, что в образце, где Tap был сверхэкспрессирован в присутствии TSi, мы не наблюдали дальнейшего увеличения (рис. 8B, рис. S4C и S4D). Напротив, когда Sam68 сверхэкспрессировался в клетках с истощением Tpr, мы наблюдали умеренное синергетическое увеличение p24. Кроме того, анализ уровней РНК Gag/Pol-CTE в этих образцах с помощью количественной ПЦР в реальном времени продемонстрировал ту же тенденцию (фиг. 8C). Истощение Tpr само по себе увеличивало уровни РНК Gag/Pol как в ядре, так и в цитоплазме, которые существенно не менялись при сверхэкспрессии Tap (рис.8С). Это не очень удивительно, так как показано, что Tap улучшает цитоплазматическую утилизацию Gag/Pol-CTE РНК, что может происходить только после ее экспорта [34]. Однако, когда Sam68 был сверхэкспрессирован в образцах с истощением Tpr, мы наблюдали значительное увеличение уровней РНК Gag/Pol (рис. 8C), что, в свою очередь, отражалось в повышенных уровнях p24 (рис. 8B). Основываясь на этих результатах, мы полагаем, что и Tpr, и Sam68 регулируют экспорт несплайсированной РНК на разных стадиях, а комбинаторный эффект истощения и сверхэкспрессии приводит к синергетическому эффекту.
Однако, когда Sam68 был сверхэкспрессирован в образцах с истощением Tpr, мы наблюдали значительное увеличение уровней РНК Gag/Pol (рис. 8C), что, в свою очередь, отражалось в повышенных уровнях p24 (рис. 8B). Основываясь на этих результатах, мы полагаем, что и Tpr, и Sam68 регулируют экспорт несплайсированной РНК на разных стадиях, а комбинаторный эффект истощения и сверхэкспрессии приводит к синергетическому эффекту.
Рис. 8. Сверхэкспрессия Sam68 в клетках с истощением Tpr приводит к синергетическому увеличению экспорта несплайсированной РНК.
(A) Через 48 часов после трансфекции NS-Si и TSi клетки HEK293T повторно трансфицировали теми же олигонуклеотидами siRNA вместе с плазмидами Gag/Pol-CTE и CMV-β-Gal и 2 мкг HA-Sam68 или HA -Tap/Nxf1конструирует. Полученные таким образом лизаты анализировали с помощью иммуноблота на нокдаун Tpr и сверхэкспрессию HA-Sam68 и HA-Tap (B). В лизатах оценивали уровень экспрессии p24 и β-Gal, и полученные значения нормализовали.(C) ПЦР-анализ в реальном времени мРНК, выделенной из ядерных и цитоплазматических фракций клеток HEK293T, совместно трансфицированных либо NS-Si, либо TSi вместе с конструкциями HA-Sam68 или HA-Tap/Nxf1 и репортерной плазмидой Gag/Pol-CTE.
https://doi.org/10.1371/journal.pone.0029921.g008
Нуклеопорин Nup153, заякоривающий белок Tpr, также участвует в регуляции экспорта несплайсированной РНК
Наши результаты к настоящему времени твердо установили роль Tpr в регуляции CTE-опосредованного экспорта несплайсированной РНК.Однако существует вероятность того, что помимо Tpr в эту модуляцию могут быть вовлечены и другие нуклеопорины, которые, как известно, играют роль в ядерно-цитоплазматическом транспорте. Нуклеопорины с консервативными повторами FXFG (фенилаланин и глицин) в своей последовательности играют важную роль в опосредовании ядерно-цитоплазматического транспорта, обеспечивая интерфейс взаимодействия, который способствует перемещению комплексов рецептор-груз через NPC [41]. Для этого исследования были рассмотрены различные нуклеопорины, содержащие FG-повторы, такие как Nup214, Nup358/RanBP2, локализованные в цитоплазматических фибриллах NPC, и Nup153, Nup98 и Nup50, присутствующие на нуклеоплазматической стороне NPC. Специфические миРНК использовали для индивидуального истощения вышеупомянутых нуклеопоринов (фиг. 9А) и количественно определяли экспорт Gag/Pol-CTE РНК путем измерения нормализованных уровней р24 в белковых экстрактах. В то время как мы наблюдали повышенные уровни нормализованной экспрессии p24 в образцах, когда либо Tpr, либо Nup153 были истощены, истощение других FG, содержащих нуклеопорины, не имело эффекта (рис. 9B, рис. S5A и S5B). Сообщалось, что взаимодействие между Tpr и Nup153 необходимо для локализации Tpr в ядерной поре [7].Если повышенный экспорт Gag/Pol-CTE РНК, наблюдаемый при истощении Nup153, является независимой функцией Nup153, мы ожидаем кумулятивного увеличения при истощении как Tpr, так и Nup153. Мы наблюдали повышенные уровни p24, когда либо Tpr, либо Nup153 истощены, при этом истощение Tpr повышало уровни p24 более эффективно, чем истощение Nup153 (рис. 9C и 9D, рис. S5C и S5D). Однако мы не наблюдали кумулятивного повышения уровней p24, когда оба они были истощены, скорее, мы обнаружили уровни p24, аналогичные тем, которые наблюдались при нокдауне Tpr отдельно.
Специфические миРНК использовали для индивидуального истощения вышеупомянутых нуклеопоринов (фиг. 9А) и количественно определяли экспорт Gag/Pol-CTE РНК путем измерения нормализованных уровней р24 в белковых экстрактах. В то время как мы наблюдали повышенные уровни нормализованной экспрессии p24 в образцах, когда либо Tpr, либо Nup153 были истощены, истощение других FG, содержащих нуклеопорины, не имело эффекта (рис. 9B, рис. S5A и S5B). Сообщалось, что взаимодействие между Tpr и Nup153 необходимо для локализации Tpr в ядерной поре [7].Если повышенный экспорт Gag/Pol-CTE РНК, наблюдаемый при истощении Nup153, является независимой функцией Nup153, мы ожидаем кумулятивного увеличения при истощении как Tpr, так и Nup153. Мы наблюдали повышенные уровни p24, когда либо Tpr, либо Nup153 истощены, при этом истощение Tpr повышало уровни p24 более эффективно, чем истощение Nup153 (рис. 9C и 9D, рис. S5C и S5D). Однако мы не наблюдали кумулятивного повышения уровней p24, когда оба они были истощены, скорее, мы обнаружили уровни p24, аналогичные тем, которые наблюдались при нокдауне Tpr отдельно.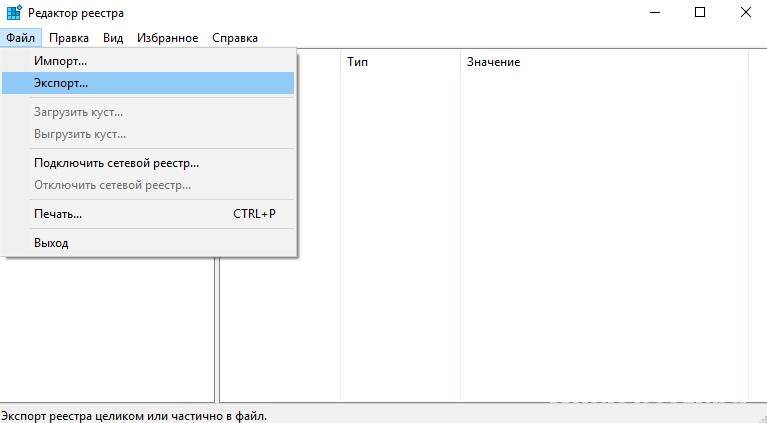 Эти результаты предполагают, что Tpr и Nup153 оба регулируют экспорт несплайсированной РНК и, скорее всего, они функционируют одним и тем же путем.
Эти результаты предполагают, что Tpr и Nup153 оба регулируют экспорт несплайсированной РНК и, скорее всего, они функционируют одним и тем же путем.
Рис. 9. Нуклеопорин Nup153, белок, закрепляющий Tpr, также участвует в регуляции экспорта несплайсированной РНК.
(A) Клетки HEK293T трансфицировали миРНК против различных нуклеопоринов вместе с конструкциями Gag/Pol-CTE и CMV-β-Gal. Вестерн-блоттинг клеточных экстрактов, подтверждающий истощение различных нуклеопоринов при обработке соответствующими миРНК.(B) Через 48 часов после трансфекции в лизатах оценивали количество экспрессии p24 и β-Gal и нормализовали полученные значения. (C) Клетки трансфицировали миРНК против Nup153 или Tpr или Nup153+Tpr вместе с конструкциями Gag/Pol-CTE и CMV-β-Gal. Вестерн-блоттинг клеточных экстрактов, подтверждающий истощение Nup153 и Tpr при обработке соответствующими миРНК. (D) Количество нормализованной экспрессии р24 оценивали в лизатах.
https://doi.org/10.1371/journal. pone.0029921.g009
pone.0029921.g009
Локализация Tpr в комплексе Nucleopore необходима для регуляции экспорта, опосредованного CTE
Чтобы определить область Tpr, которая необходима и достаточна для регуляции экспорта несплайсированной РНК, мы создали серию устойчивых к siRNA делеционных конструкций Tpr (рис. S6A). Результаты показали, что только N-концевой фрагмент и фрагмент Tpr-NM, содержащий как N-, так и срединную области, были способны восстановить фенотип (рис.S6B и S6C). Ранее было показано, что Tpr обладает сигналом ядерной локализации в карбоксиконцевой области, а N-концевой фрагмент, как сообщается, содержит домен, ассоциированный с NPC [28]. Когда мы провели иммунофлуоресцентный анализ, чтобы установить субклеточную локализацию различных фрагментов Tpr, мы обнаружили, что TprN и NM в основном локализуются в цитозоле (рис. S6E). Однако мы не можем исключить возможность того, что по крайней мере некоторые количества TprN и TprNM могут ассоциироваться с NPC, даже если они не локализуются внутри ядра. Другая возможность заключается в том, что сверхэкспрессия TprN и TprNM в сочетании с их преимущественно цитозольной локализацией может приводить к тому, что другие до сих пор неизвестные клеточные факторы, необходимые для CTE-опосредованного экспорта несплайсированной РНК и последующей экспрессии генов, титруются TprN и TprNM. Кроме того, мы наблюдали аномальные ядерные пузыри, когда TprN и TprNM сверхэкспрессированы, и это также может влиять на CTE-опосредованный экспорт РНК. Эти аспекты необходимо дополнительно изучить, прежде чем можно будет сделать какие-либо окончательные выводы, поскольку некоторые из эффектов могут быть фенотипами сверхэкспрессии.
Другая возможность заключается в том, что сверхэкспрессия TprN и TprNM в сочетании с их преимущественно цитозольной локализацией может приводить к тому, что другие до сих пор неизвестные клеточные факторы, необходимые для CTE-опосредованного экспорта несплайсированной РНК и последующей экспрессии генов, титруются TprN и TprNM. Кроме того, мы наблюдали аномальные ядерные пузыри, когда TprN и TprNM сверхэкспрессированы, и это также может влиять на CTE-опосредованный экспорт РНК. Эти аспекты необходимо дополнительно изучить, прежде чем можно будет сделать какие-либо окончательные выводы, поскольку некоторые из эффектов могут быть фенотипами сверхэкспрессии.
Было показано, что Nup153 взаимодействует с Tpr, и это взаимодействие опосредовано остатками L458 и M489 в N-концевой спиральной области Tpr. Было показано, что взаимодействие необходимо для локализации Tpr [7]. Тот факт, что мы не наблюдали кумулятивного эффекта при двойном нокдауне Tpr и Nup153, и что фрагмент Tpr-NM восстанавливал фенотип, позволяет предположить, что опосредованное Nup153 заякоривание Tpr может быть важным для модулирования экспорта РНК Gag/Pol-CTE. Чтобы проверить это, мы создали устойчивый к миРНК мутант Tpr с дефицитом локализации (Tpr-L458P/M489P).Как и ожидалось, FLAG-Tpr-Si был локализован в ядерной мембране (фиг. 10А). Однако, в соответствии с более ранними сообщениями [7], локализация мутанта Tpr-L458P/M489P-Si была внутриядерной (Fig. 10A и S7A). Как и ожидалось, когда клетки трансфицировали конструкцией FLAG-Tpr-Si, устойчивой к миРНК, мы наблюдали снижение уровней p24 (фиг. 10B, фиг. S7B и S7C). Важно отметить, что присутствие устойчивых к миРНК FLAG-Tpr-L458P/M489P-Si не снижало уровень нормализованного p24, хотя его экспрессия была аналогична FLAG-Tpr-Si (рис.10В и 10С). Взятые вместе, эти результаты предоставляют убедительные доказательства того, что локализация Tpr в NPC является критической для регуляции экспорта интрон-содержащей РНК.
Чтобы проверить это, мы создали устойчивый к миРНК мутант Tpr с дефицитом локализации (Tpr-L458P/M489P).Как и ожидалось, FLAG-Tpr-Si был локализован в ядерной мембране (фиг. 10А). Однако, в соответствии с более ранними сообщениями [7], локализация мутанта Tpr-L458P/M489P-Si была внутриядерной (Fig. 10A и S7A). Как и ожидалось, когда клетки трансфицировали конструкцией FLAG-Tpr-Si, устойчивой к миРНК, мы наблюдали снижение уровней p24 (фиг. 10B, фиг. S7B и S7C). Важно отметить, что присутствие устойчивых к миРНК FLAG-Tpr-L458P/M489P-Si не снижало уровень нормализованного p24, хотя его экспрессия была аналогична FLAG-Tpr-Si (рис.10В и 10С). Взятые вместе, эти результаты предоставляют убедительные доказательства того, что локализация Tpr в NPC является критической для регуляции экспорта интрон-содержащей РНК.
Рисунок 10. Локализация Tpr в комплексе Nucleopore важна для регуляции экспорта, опосредованного CTE.
(A) Иммунофлуоресцентный анализ клеток 293T, трансфицированных конструкциями Flag-Tpr или Flag-Tpr-L458P/M489P-Si. (B) Клетки 293T котрансфицировали NS-Si или TSi или Nup153-siRNA вместе с репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal и 2 мкг Tpr-Si или Flag-Tpr-L458P/ Конструкции M489P-Si (Tpr-LM-Si).Вестерн-блот-анализ, указывающий на сходные уровни экспрессии конструкций Tpr-Si и Tpr-LM-Si после истощения эндогенного Tpr. (C) Анализировали уровни p24 и β-галактозидазы в экстрактах цельных клеток каждого из образцов. Затем значения p24 корректировали с учетом вариаций показаний β-Gal.
(B) Клетки 293T котрансфицировали NS-Si или TSi или Nup153-siRNA вместе с репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal и 2 мкг Tpr-Si или Flag-Tpr-L458P/ Конструкции M489P-Si (Tpr-LM-Si).Вестерн-блот-анализ, указывающий на сходные уровни экспрессии конструкций Tpr-Si и Tpr-LM-Si после истощения эндогенного Tpr. (C) Анализировали уровни p24 и β-галактозидазы в экстрактах цельных клеток каждого из образцов. Затем значения p24 корректировали с учетом вариаций показаний β-Gal.
https://doi.org/10.1371/journal.pone.0029921.g010
Обсуждение
За последние несколько лет несколько групп сосредоточили свои исследования на клеточных функциях нуклеопоринов, включая те, которые локализованы в области ядерной корзины, такие как Tpr и Nup153.Было показано, что Tpr активирует контрольную точку митотического веретена [16], а его ассоциация с динеиновым комплексом важна для правильной сегрегации хромосом во время митоза [17]. Недавнее исследование показало, что нуклеопорин Tpr важен для установления перинуклеарных зон исключения гетерохроматина [42]. Эти наблюдения подразумевают критическую роль человеческого белка Tpr в модулировании разнообразных функций. Однако роль нуклеопорина Tpr в ядерно-цитоплазматическом транспорте макромолекул изучена недостаточно.Исследования, проведенные с дрожжевым гомологом Tpr, Mlp1, выявили роль этого белка в удержании в ядре несплайсированной РНК [30].
Эти наблюдения подразумевают критическую роль человеческого белка Tpr в модулировании разнообразных функций. Однако роль нуклеопорина Tpr в ядерно-цитоплазматическом транспорте макромолекул изучена недостаточно.Исследования, проведенные с дрожжевым гомологом Tpr, Mlp1, выявили роль этого белка в удержании в ядре несплайсированной РНК [30].
В клетках млекопитающих транскрипты мРНК с несплайсированными интронами ограничены ядром. Ретровирусы преодолевают это удержание и экспортируют свою полноразмерную геномную РНК, содержащую интроны, с помощью -цис--действующих элементов, таких как RRE (и белок-трансактиватор Rev) или CTE [24], [43], [44]. Мы наблюдали значительное усиление функции CTE в клетках 293T, лишенных Tpr, что позволяет предположить, что Tpr играет критическую роль в ограничении CTE-опосредованного экспорта интрон-содержащей РНК.Тот факт, что транспорт белка, распределение мРНК поли(А) + и Rev-опосредованный экспорт несплайсированной РНК оставались неизменными при нокдауне Tpr, указывает на то, что Tpr может специфически взаимодействовать прямо или косвенно с комплексами CTE-mRNP, чтобы модулировать их экспорт через NPC. Более того, увеличение уровня ядерной CTE-РНК, наблюдаемое в отсутствие Tpr, также указывает на то, что этот нуклеопорин может играть дополнительную роль в регуляции процессинга этих транскриптов.
Более того, увеличение уровня ядерной CTE-РНК, наблюдаемое в отсутствие Tpr, также указывает на то, что этот нуклеопорин может играть дополнительную роль в регуляции процессинга этих транскриптов.
Sam68, Nxt1/p15 и Tap/Nxf1 играют роль в усилении функции CTE [26], [33], [34], [45]. Образование гетеродимеров Tap и Nxt усиливает связывание нуклеопоринов с Tap и приводит к усилению его ядерно-цитоплазматического челнока [46]. Ассоциация Nxt1 с мРНК Tap-CTE усиливает взаимодействие комплекса мРНП с NPC, что приводит к его эффективному экспорту [47]. Было также показано, что эти белки способствуют полирибосомной ассоциации интрон-содержащих РНК, что приводит к их эффективной трансляции [34].Поскольку истощение Tpr и экспрессия Sam68, Tap и Nxt1 регулируют экспорт несплайсированной РНК, мы исследовали возможность прямого взаимодействия между Tpr и Tap, Nxt1 или Sam68. Хотя мы наблюдали взаимодействие между эндогенным Tpr с иммунопреципитированным ERK2 [22], мы не смогли обнаружить никакого взаимодействия Tpr с белками Sam68, Tap или Nxt1 (рис. S8). Было показано, что Tap/Nxf1 влияет на экспорт мРНК из ядра в различных модельных системах [37], [38], [39], [40]. В нашем исследовании при частичном истощении Tap мы наблюдали небольшое снижение уровней p24 и β-GAL (рис.7А и 7В). Однако, когда Tap был эффективно истощен (рис. 7C-E), в соответствии с предыдущими выводами, мы наблюдали существенное снижение показателей β-GAL. Напротив, истощение Tap или Tap и Tpr вместе значительно не изменяет уровни p24 по сравнению с уровнями, наблюдаемыми при истощении только Tpr, что позволяет предположить, что изменение уровней Tpr достаточно для высвобождения комплексов CTE-mRNP в цитозоль. . Кроме того, мы наблюдали, что одновременное истощение Tpr и избыточная экспрессия Sam68 приводили к синергетическому увеличению экспорта несплайсированной РНК.Эти результаты показывают, что способ регуляции экспорта несплайсированной РНК с помощью Sam68 и Tpr, вероятно, различается. Как было показано ранее, Sam68, скорее всего, необходим для стабилизации мРНК и улучшения цитозольной утилизации несплайсированной РНК [26], в то время как функция Tpr опосредуется и может быть опосредована либо прямым взаимодействием, либо через какой-то неидентифицированный РНК-связывающий белок.
S8). Было показано, что Tap/Nxf1 влияет на экспорт мРНК из ядра в различных модельных системах [37], [38], [39], [40]. В нашем исследовании при частичном истощении Tap мы наблюдали небольшое снижение уровней p24 и β-GAL (рис.7А и 7В). Однако, когда Tap был эффективно истощен (рис. 7C-E), в соответствии с предыдущими выводами, мы наблюдали существенное снижение показателей β-GAL. Напротив, истощение Tap или Tap и Tpr вместе значительно не изменяет уровни p24 по сравнению с уровнями, наблюдаемыми при истощении только Tpr, что позволяет предположить, что изменение уровней Tpr достаточно для высвобождения комплексов CTE-mRNP в цитозоль. . Кроме того, мы наблюдали, что одновременное истощение Tpr и избыточная экспрессия Sam68 приводили к синергетическому увеличению экспорта несплайсированной РНК.Эти результаты показывают, что способ регуляции экспорта несплайсированной РНК с помощью Sam68 и Tpr, вероятно, различается. Как было показано ранее, Sam68, скорее всего, необходим для стабилизации мРНК и улучшения цитозольной утилизации несплайсированной РНК [26], в то время как функция Tpr опосредуется и может быть опосредована либо прямым взаимодействием, либо через какой-то неидентифицированный РНК-связывающий белок. Было показано, что у дрожжей РНК-связывающие белки Yra1p и Nab2p необходимы для стыковки комплексов мРНП вблизи экспортных ворот Mlp, расположенных на ядерной мембране [35].Недавнее исследование показало, что истощение РНК-эндонуклеазного белка Swt1 приводит к накоплению ядерной поли(А)+ мРНК и усилению цитоплазматической утечки несплайсированных пре-мРНК у мутантов mlp1Δ и nup60Δ [48]. Гомологи Swt1 у человека, белки Smg5 и Smg6, которые, как было показано, играют роль в нонсенс-опосредованном распаде мРНК [49], [50], [51]. Наши предварительные данные с истощением белков Smg5 и Smg6 в клетках с нокдауном Tpr для изучения CTE-зависимого экспорта несплайсированной РНК не выявили значительного эффекта этих белков (данные не показаны).Будущие исследования будут направлены на изучение роли гомологов дрожжевых белков у млекопитающих в регуляции опосредованного Tpr экспорта несплайсированной РНК.
Было показано, что у дрожжей РНК-связывающие белки Yra1p и Nab2p необходимы для стыковки комплексов мРНП вблизи экспортных ворот Mlp, расположенных на ядерной мембране [35].Недавнее исследование показало, что истощение РНК-эндонуклеазного белка Swt1 приводит к накоплению ядерной поли(А)+ мРНК и усилению цитоплазматической утечки несплайсированных пре-мРНК у мутантов mlp1Δ и nup60Δ [48]. Гомологи Swt1 у человека, белки Smg5 и Smg6, которые, как было показано, играют роль в нонсенс-опосредованном распаде мРНК [49], [50], [51]. Наши предварительные данные с истощением белков Smg5 и Smg6 в клетках с нокдауном Tpr для изучения CTE-зависимого экспорта несплайсированной РНК не выявили значительного эффекта этих белков (данные не показаны).Будущие исследования будут направлены на изучение роли гомологов дрожжевых белков у млекопитающих в регуляции опосредованного Tpr экспорта несплайсированной РНК.
повтора FG, содержащие нуклеопорины в NPC, необходимы для транспорта макромолекул через ядерную пору [41], [52]. Было показано, что члены суперсемейства кариоферин/импортин, рецептор экспорта мРНК Mex67/Mtr2 и транспортер Ran Ntf2 специфически взаимодействуют с FG Nups [53], [54]. Мы не обнаружили повышенных уровней p24, когда мы истощили Nup98, Nup214, Nup358 и Nup50.Nup98 представляет собой нуклеопорин, который, как было показано, связывается с внутриядерными филаментами Tpr [11]. Powers и соавт. показали, что инъекция моноспецифических поликлональных антител против Nup98 в ядро ингибирует экспорт нескольких классов РНК, включая мРНК [55]. Также было показано, что Nup98 взаимодействует с транспортными факторами мРНК, такими как Rae1 и Tap/Mex67 [39], [56]. Мы наблюдали, что истощение Nup98, опосредованное siRNA, существенно не влияло ни на показания p24, ни на β-GAL (рис. S5A и S5B), что позволяет предположить, что Nup98 не играет значительной роли в экспорте несплайсированных РНК или мРНК.Различия, обнаруженные в наших наблюдениях, могут быть связаны с различиями в методах исследования. Однако необходимо провести систематическое исследование с использованием нескольких методов, чтобы определить роль, которую Nup98 играет в экспорте мРНК.
Было показано, что члены суперсемейства кариоферин/импортин, рецептор экспорта мРНК Mex67/Mtr2 и транспортер Ran Ntf2 специфически взаимодействуют с FG Nups [53], [54]. Мы не обнаружили повышенных уровней p24, когда мы истощили Nup98, Nup214, Nup358 и Nup50.Nup98 представляет собой нуклеопорин, который, как было показано, связывается с внутриядерными филаментами Tpr [11]. Powers и соавт. показали, что инъекция моноспецифических поликлональных антител против Nup98 в ядро ингибирует экспорт нескольких классов РНК, включая мРНК [55]. Также было показано, что Nup98 взаимодействует с транспортными факторами мРНК, такими как Rae1 и Tap/Mex67 [39], [56]. Мы наблюдали, что истощение Nup98, опосредованное siRNA, существенно не влияло ни на показания p24, ни на β-GAL (рис. S5A и S5B), что позволяет предположить, что Nup98 не играет значительной роли в экспорте несплайсированных РНК или мРНК.Различия, обнаруженные в наших наблюдениях, могут быть связаны с различиями в методах исследования. Однако необходимо провести систематическое исследование с использованием нескольких методов, чтобы определить роль, которую Nup98 играет в экспорте мРНК.
Интересно, что истощение Nup153, повтора FG, содержащего нуклеопорин, который играет критическую роль в различных клеточных процессах, включая развитие клеточного цикла [57], приводило к повышению уровня p24. Показано, что сверхэкспрессия Nup153 вызывает накопление мРНК поли(А) + в ядре [58], а инъекция антител против Nup153 блокирует опосредованный NES экспорт белков, мяРНК U1, 5sРНК и сплайсированных мРНК [59].Наблюдаемое увеличение уровней p24 при истощении Nup153, хотя и значительное, не было столь эффективным, как наблюдаемое при истощении Tpr. Комбинированный нокдаун Nup153 и Tpr не показал синергетического эффекта на уровни p24, что указывает на то, что оба они, скорее всего, функционируют по одному и тому же пути. В предыдущем исследовании было показано, что Nup153 необходим для закрепления Tpr на NPC [7], а остатки L458 и M489 в N-концевой области Tpr необходимы для их взаимодействия.В совокупности эффект, проявляемый Nup153 на CTE-опосредованный экспорт, может быть связан с возможностью того, что истощение Nup153 предотвращает или дестабилизирует связывание NPC с Tpr, и демонстрирует, что ассоциация Tpr с NPC является критической для его функции. Результаты, которые мы получили с мутантным Tpr с дефицитом локализации, после чего неправильная локализация Tpr внутрь ядра привела к неспособности регулировать экспорт РНК, позволяют предположить, что перинуклеарная локализация Tpr является важным шагом в регуляции CTE-опосредованного экспорта.
Результаты, которые мы получили с мутантным Tpr с дефицитом локализации, после чего неправильная локализация Tpr внутрь ядра привела к неспособности регулировать экспорт РНК, позволяют предположить, что перинуклеарная локализация Tpr является важным шагом в регуляции CTE-опосредованного экспорта.
Пока эта рукопись находилась в стадии подготовки, группа Hammarskjold сообщила, что Tpr регулирует экспорт мРНК с помощью -цис--действующего CTE-элемента и что Tpr не влияет на транспорт интрон-содержащих мРНК через путь Crm1 [60]. Авторы также показали, что спасение с помощью устойчивой к siRNA формы Tpr подавляет эффект CTE-опосредованного экспорта и что совместная экспрессия Sam68 и Tpr-shRNA приводит к значительному усилению экспрессии p24. Эти результаты подтверждают наши выводы [60].Авторы предполагают, что аддитивный эффект, наблюдаемый при сверхэкспрессии Sam68 и нокдауне Tpr, может быть связан с перекрестными разговорами между двумя белками, однако в нашем исследовании мы не обнаружили прямого взаимодействия между Tpr и Sam68 (рис.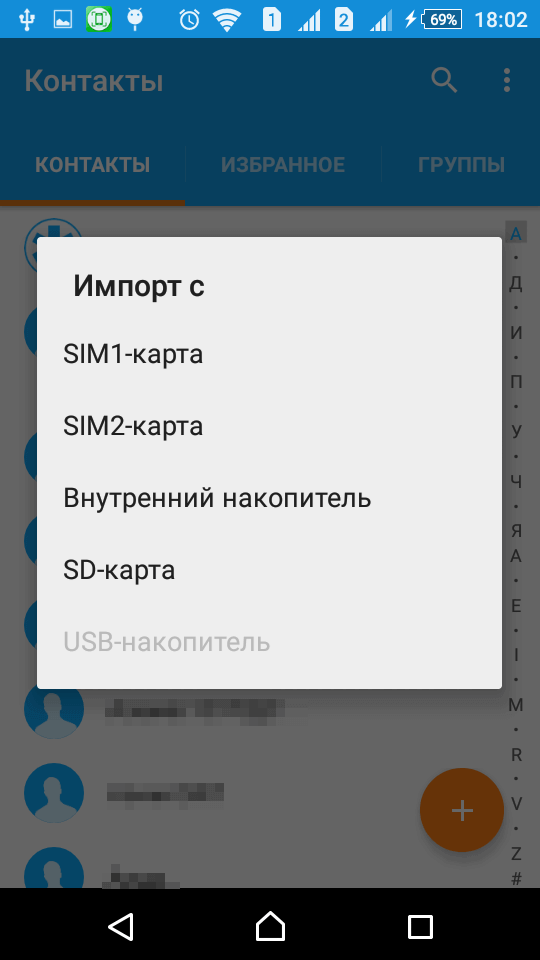 S8). Основываясь на своих экспериментальных результатах, Coyle et al. также предполагают, что свежеобразованные молекулы Tpr, которые составляют минорные, но динамичные пулы ядерных белков Tpr, которые участвуют в регуляции транскрипции комплексов CTE-mRNP, достаточны для усиления экспрессии p24.Тот факт, что мы наблюдаем увеличение ядерных уровней CTE-мРНК при истощении Tpr, подтверждает эту гипотезу. Результаты наших экспериментов с нокдауном, опосредованным Nup153 siRNA, а также исследования мутантов по локализации Tpr показывают, что Tpr, локализованный в NPC, играет критическую роль в регуляции экспорта несплайсированной РНК. Помимо регуляторной роли Tpr в ядерном экспорте, авторы сообщают, что истощение Tpr приводит к усилению ассоциации комплексов CTE-mRNP в полирибосомных комплексах, демонстрируя роль нуклеопорина Tpr в цитоплазме.Однако истощение Tpr не влияло на стабильность белка Gag/Pol в цитозоле. Хотя наше исследование не рассматривает возможную роль Tpr в цитоплазме, увеличение пула ядерных CTE-мРНК при истощении Tpr (Fig.
S8). Основываясь на своих экспериментальных результатах, Coyle et al. также предполагают, что свежеобразованные молекулы Tpr, которые составляют минорные, но динамичные пулы ядерных белков Tpr, которые участвуют в регуляции транскрипции комплексов CTE-mRNP, достаточны для усиления экспрессии p24.Тот факт, что мы наблюдаем увеличение ядерных уровней CTE-мРНК при истощении Tpr, подтверждает эту гипотезу. Результаты наших экспериментов с нокдауном, опосредованным Nup153 siRNA, а также исследования мутантов по локализации Tpr показывают, что Tpr, локализованный в NPC, играет критическую роль в регуляции экспорта несплайсированной РНК. Помимо регуляторной роли Tpr в ядерном экспорте, авторы сообщают, что истощение Tpr приводит к усилению ассоциации комплексов CTE-mRNP в полирибосомных комплексах, демонстрируя роль нуклеопорина Tpr в цитоплазме.Однако истощение Tpr не влияло на стабильность белка Gag/Pol в цитозоле. Хотя наше исследование не рассматривает возможную роль Tpr в цитоплазме, увеличение пула ядерных CTE-мРНК при истощении Tpr (Fig.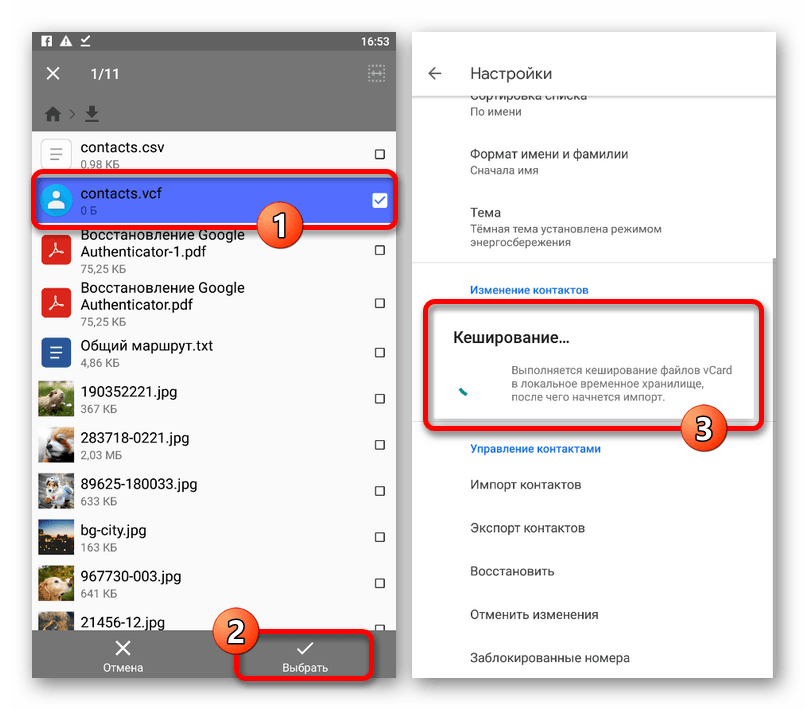 6) указывает на роль Tpr в нуклеоплазме. Объединяя результаты обоих исследований, оказывается, что регуляция CTE-опосредованного экспорта несплайсированной РНК представляет собой сложное и контролируемое явление, включающее множество белков, действующих на различных уровнях в ядре, из которых нуклеопорин Tpr является важным модулятором.Будущие исследования будут направлены на идентификацию ключевых РНК-связывающих белков, взаимодействующих с Tpr, и на расшифровку точного механизма, с помощью которого Tpr модулирует CTE-зависимый экспорт несплайсированной РНК.
6) указывает на роль Tpr в нуклеоплазме. Объединяя результаты обоих исследований, оказывается, что регуляция CTE-опосредованного экспорта несплайсированной РНК представляет собой сложное и контролируемое явление, включающее множество белков, действующих на различных уровнях в ядре, из которых нуклеопорин Tpr является важным модулятором.Будущие исследования будут направлены на идентификацию ключевых РНК-связывающих белков, взаимодействующих с Tpr, и на расшифровку точного механизма, с помощью которого Tpr модулирует CTE-зависимый экспорт несплайсированной РНК.
Материалы и методы
Плазмидные конструкции и олигонуклеотиды миРНК
Олигонуклеотиды миРНК (таблица S1) были приобретены либо у Dharmacon, либо у Invitrogen. Конструкции pCMV-Gag/Pol-CTE, pCMV-Gag/PR-RRE и pCMV-β-Gal были любезно предоставлены Dr. Marie-Louise Hammarskjold Coyle [26] (Университет Вирджинии), Dr.Ханс-Георг Крауслих [33] (Гамбургский университет) и доктор Сагар Сенгупта (Национальный институт иммунологии) соответственно.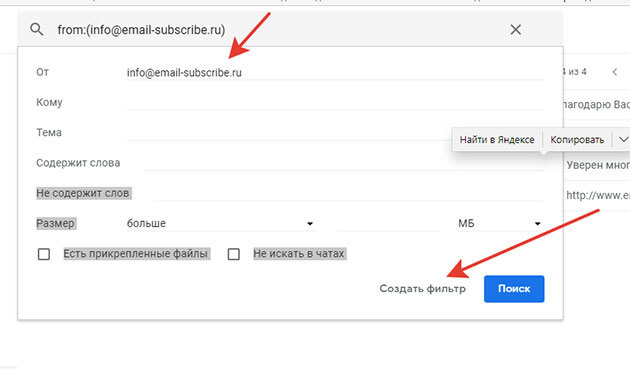 Клетки HEK293T, COS-1 и HeLa были получены от ATCC, США.
Клетки HEK293T, COS-1 и HeLa были получены от ATCC, США.
Ранее сообщалось о конструировании плазмиды pcDNA3-FLAG-TprFL [22]. Клоны Tpr-Si и Tpr-L458P/M489P были созданы путем перекрывающейся ПЦР с использованием специфических праймеров. Конструкцию Luc-CTE получали путем амплификации 5′-области сайта сплайсинга и 3′-области сайта сплайсинга, области СТЕ и гена люциферазы и их клонирования в pcDNA3.1 вектор. FLAG-Rev и HA-Tap были созданы путем амплификации кодирующих областей и их клонирования в векторы pcDNA3-FLAG и pcDNA3-HA соответственно. Клон HA-Sam68 был получен от Addgene (плазмида 17688; [61]).
Культура клеток, трансфекция и создание стабильных клеточных линий
Клетки HEK293T, COS-1 и HeLa выращивали в среде DMEM с добавлением 10% эмбриональной бычьей сыворотки (FBS). Все трансфекции в клетках HEK293T проводили в 6-луночных планшетах с использованием метода с фосфатом кальция. Трансфекции в клетках HeLa и COS-1 проводили с использованием липофектамина 2000 (Invitrogen) в соответствии с рекомендациями производителя.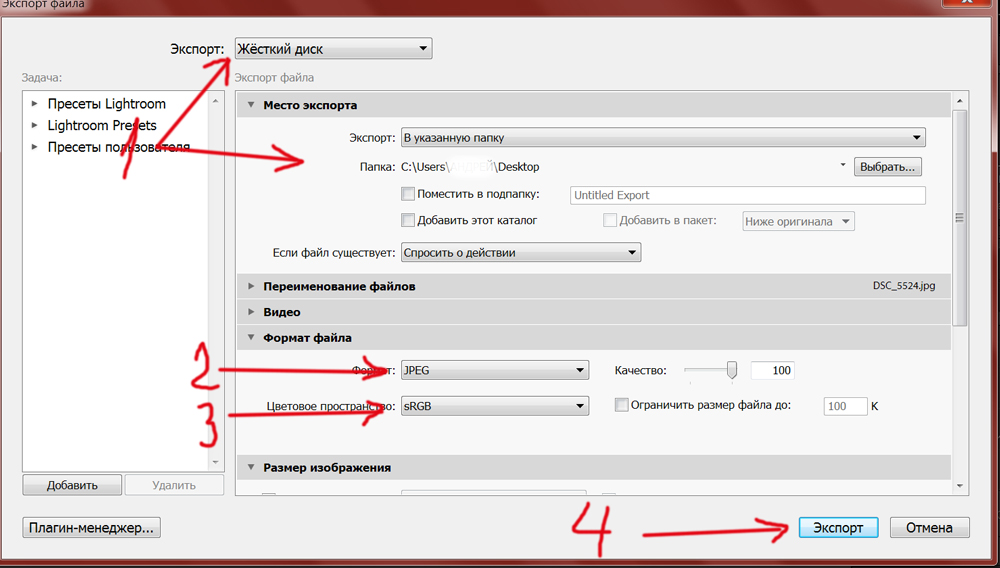 Для анализа CTE-опосредованного экспорта клетки трансфицировали 250 нг pCMV-Gag/Pol-CTE, 100 нг pCMV-β-Gal и 1 мкг соответствующей siRNA. Во всех трансфекциях конечное количество плазмидной ДНК, присутствующей в смеси для трансфекции, выравнивали добавлением соответствующего количества вектора pCDNA3-FLAG. Клетки собирали через 48 часов после трансфекции для дальнейшего анализа, если не указано иное. Стабильные клеточные линии FLAG-Tpr и FLAG-Tpr-Si получали путем трансфекции этих конструкций в клетки HEK293T с использованием липофектамина 2000 (Invitrogen).Через 24 часа после трансфекции 10 4 клеток высевали в чашку диаметром 100 мм в среду, содержащую 600 мкг/мл генетицина (Invitrogen), и инкубировали в течение 10 дней. Полученные колонии индивидуально размножали и проверяли на экспрессию введенных генов с помощью вестерн-блоттинга и непрямого иммунофлуоресцентного анализа с использованием антител против FLAG (Sigma).
Для анализа CTE-опосредованного экспорта клетки трансфицировали 250 нг pCMV-Gag/Pol-CTE, 100 нг pCMV-β-Gal и 1 мкг соответствующей siRNA. Во всех трансфекциях конечное количество плазмидной ДНК, присутствующей в смеси для трансфекции, выравнивали добавлением соответствующего количества вектора pCDNA3-FLAG. Клетки собирали через 48 часов после трансфекции для дальнейшего анализа, если не указано иное. Стабильные клеточные линии FLAG-Tpr и FLAG-Tpr-Si получали путем трансфекции этих конструкций в клетки HEK293T с использованием липофектамина 2000 (Invitrogen).Через 24 часа после трансфекции 10 4 клеток высевали в чашку диаметром 100 мм в среду, содержащую 600 мкг/мл генетицина (Invitrogen), и инкубировали в течение 10 дней. Полученные колонии индивидуально размножали и проверяли на экспрессию введенных генов с помощью вестерн-блоттинга и непрямого иммунофлуоресцентного анализа с использованием антител против FLAG (Sigma).
ИФА p24 и анализ β-галактозидазы
Собранные клетки лизировали буфером для лизиса M2 (50 мМ Tris-HCl, 150 мМ NaCl, 10 % глицерина, 1 % Triton X-100, 0.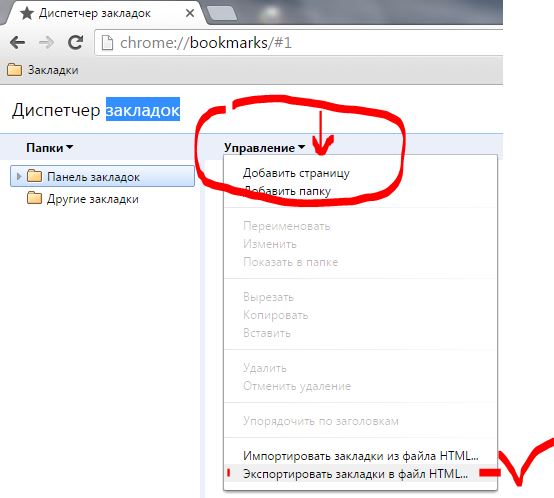 5 мМ ЭГТА, 0,5 мМ ЭДТА), содержащий коктейль ингибиторов протеазы (Roche). Лизаты осветляли высокоскоростным центрифугированием. Уровни экспрессии p24 определяли методом сэндвич-ELISA с использованием моноклональных антител против мышиного и антикроличьего p24 (полученных из программы AIDS Research and Reference Reagent). Активность β-галактозидазы (β-Gal) определяли путем инкубации лизата с 400 мкг или -нитрофенил-β-D-галактопиранозида (ONPG) в буфере Z (40 мМ Na 2 HPO 4 .7H 2 O, 60 мМ NaH 2 ПО 4 .H 2 O, 10 мМ KCl, 1 мМ MgSO 4 .7H 2 O) в течение 15–30 минут и измерение поглощения при 420 нм. Показания р24, полученные с помощью ELISA, затем нормализовали по отношению к показаниям β-галактозидазы. Данные, представленные на фигурах, представляют собой средние значения, полученные из трех независимых трансфекций; планки погрешностей представляют собой стандартное отклонение.
5 мМ ЭГТА, 0,5 мМ ЭДТА), содержащий коктейль ингибиторов протеазы (Roche). Лизаты осветляли высокоскоростным центрифугированием. Уровни экспрессии p24 определяли методом сэндвич-ELISA с использованием моноклональных антител против мышиного и антикроличьего p24 (полученных из программы AIDS Research and Reference Reagent). Активность β-галактозидазы (β-Gal) определяли путем инкубации лизата с 400 мкг или -нитрофенил-β-D-галактопиранозида (ONPG) в буфере Z (40 мМ Na 2 HPO 4 .7H 2 O, 60 мМ NaH 2 ПО 4 .H 2 O, 10 мМ KCl, 1 мМ MgSO 4 .7H 2 O) в течение 15–30 минут и измерение поглощения при 420 нм. Показания р24, полученные с помощью ELISA, затем нормализовали по отношению к показаниям β-галактозидазы. Данные, представленные на фигурах, представляют собой средние значения, полученные из трех независимых трансфекций; планки погрешностей представляют собой стандартное отклонение.
Иммуноблоттинг и иммунофлуоресценция
Моноклональные антитела мыши против Tpr (ab58344), антитела против Nup153, анти-Nup98, анти-Nup214, анти-Sam68 и анти-Tap были получены от Abcam, антитела к Nxt-1 и циклину А были получены от Santa Cruz Biotechnology. .Антитело против 53BP1 было любезно предоставлено доктором Сагаром Сенгуптой, антитела против Erk2, против LaminA/C и против тубулина были приобретены у Cell Signaling Technology. Антитело против Nup358 было любезно предоставлено доктором Дзёмоном Джозефом. Все вторичные антитела были получены от Jackson Immuno Research Laboratories. Обычно 50 мкг лизатов анализировали с помощью вестерн-блоттинга после разделения на 10% SDS-PAGE. Иммунофлуоресцентный анализ проводили с клетками, фиксированными 4% параформальдегидом, с последующей пермеабилизацией 0.1% Тритон Х-100 на 10 минут. Блокирование проводили 10% нормальной куриной сывороткой (NCS) при 4°С (12 часов) с последующей инкубацией с соответствующими антителами. Покровные стекла монтировали с использованием монтажной среды, содержащей DAPI (Vectashield), и визуализировали с помощью конфокального микроскопа Carl Zeiss Axiovision LSM 510 Meta.
.Антитело против 53BP1 было любезно предоставлено доктором Сагаром Сенгуптой, антитела против Erk2, против LaminA/C и против тубулина были приобретены у Cell Signaling Technology. Антитело против Nup358 было любезно предоставлено доктором Дзёмоном Джозефом. Все вторичные антитела были получены от Jackson Immuno Research Laboratories. Обычно 50 мкг лизатов анализировали с помощью вестерн-блоттинга после разделения на 10% SDS-PAGE. Иммунофлуоресцентный анализ проводили с клетками, фиксированными 4% параформальдегидом, с последующей пермеабилизацией 0.1% Тритон Х-100 на 10 минут. Блокирование проводили 10% нормальной куриной сывороткой (NCS) при 4°С (12 часов) с последующей инкубацией с соответствующими антителами. Покровные стекла монтировали с использованием монтажной среды, содержащей DAPI (Vectashield), и визуализировали с помощью конфокального микроскопа Carl Zeiss Axiovision LSM 510 Meta.
Анализы транспорта белков и экспорта мРНК
Клеточная линия HeLa, стабильно экспрессирующая химерный белок Rev-GFP-Glucocorticoid Receptor (RGG) [29], была любезно предоставлена Dr.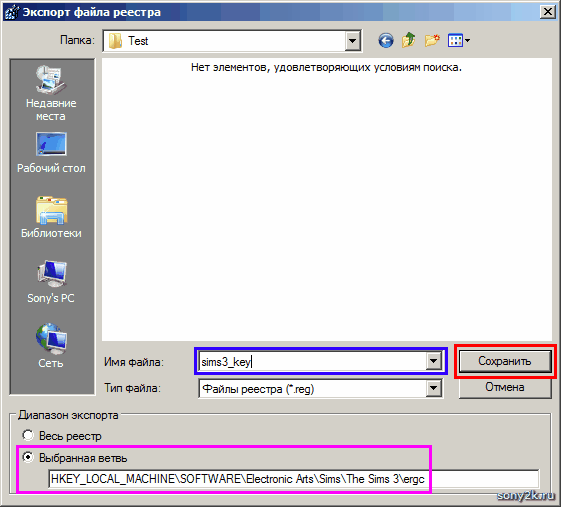 Дзёмон Джозеф. Две 60-мм чашки с указанными выше клетками (5×10 5 клеток/чашку) трансфицировали 4 мкг NS-Si или TSi. Через 24 часа после трансфекции клетки обрабатывали трипсином и высевали на покровные стекла (10 5 клеток/покровное стекло) и оставляли для восстановления на 24 часа. Мы отслеживали импорт химерного GFP, фиксируя клетки 4% параформальдегидом в разное время после обработки дексаметазоном. Для изучения ядерного экспорта клетки, обработанные 1 мкМ дексаметазона в течение 60 минут, промывали для удаления гормона и пополняли свежей средой в течение различных интервалов времени, как указано.
Дзёмон Джозеф. Две 60-мм чашки с указанными выше клетками (5×10 5 клеток/чашку) трансфицировали 4 мкг NS-Si или TSi. Через 24 часа после трансфекции клетки обрабатывали трипсином и высевали на покровные стекла (10 5 клеток/покровное стекло) и оставляли для восстановления на 24 часа. Мы отслеживали импорт химерного GFP, фиксируя клетки 4% параформальдегидом в разное время после обработки дексаметазоном. Для изучения ядерного экспорта клетки, обработанные 1 мкМ дексаметазона в течение 60 минут, промывали для удаления гормона и пополняли свежей средой в течение различных интервалов времени, как указано.
FITC-конъюгированный олигод(Т) 23-мерный зонд был получен от Integrated DNA Technologies (США) . С этим зондом проводили флуоресцентную гибридизацию in situ для анализа экспорта мРНК поли (A) + в клетках HEK293T. Через 48 часов после трансфекции миРНК для индуцирования нокдауна Tpr клетки (выращенные на покровных стеклах) фиксировали 4% параформальдегидом и пермеабилизировали 0,2% тритоном Х-100.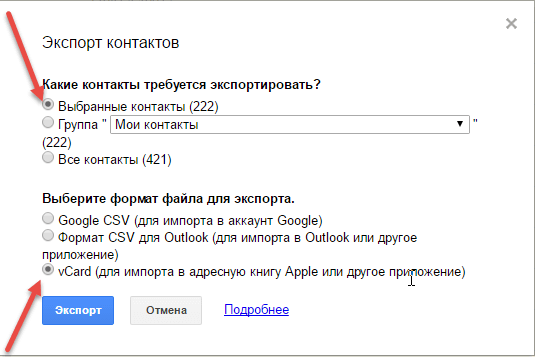 Клетки инкубировали во влажной камере в течение 3 ч при 37°С с гибридизационной смесью, содержащей 20× SSC, 50% сульфат декстрана, 1 мкг/мкл тРНК дрожжей и 1 пмоль/мкл меченого зонда.Строгие промывки после гибридизации проводили с 4× SSC и 0,1% Tween 20. Блокирование осуществляли с помощью 10% нормальной куриной сыворотки (NCS) с последующей инкубацией с соответствующими антителами.
Клетки инкубировали во влажной камере в течение 3 ч при 37°С с гибридизационной смесью, содержащей 20× SSC, 50% сульфат декстрана, 1 мкг/мкл тРНК дрожжей и 1 пмоль/мкл меченого зонда.Строгие промывки после гибридизации проводили с 4× SSC и 0,1% Tween 20. Блокирование осуществляли с помощью 10% нормальной куриной сыворотки (NCS) с последующей инкубацией с соответствующими антителами.
Выделение РНК и qRT-PCR
клетки HEK293T собирали через 48 часов после трансфекции либо NS-Si, либо TSi. Клетки лизировали в гипотоническом буфере для лизиса (20 мМ HEPES-NaOH, 2 мМ EGTA и 2 мМ MgCl 2 ) в течение 10 минут, а затем центрифугировали при 1200 об/мин для осаждения ядер и получения цитоплазматической фракции в качестве супернатанта.Ядерный осадок однократно промывали в буфере для фракционирования клеток (набор PARIS, Ambion). Лизис ядер и получение РНК как из цитозольных, так и из ядерных экстрактов проводили с использованием набора PARIS в соответствии с рекомендациями производителя.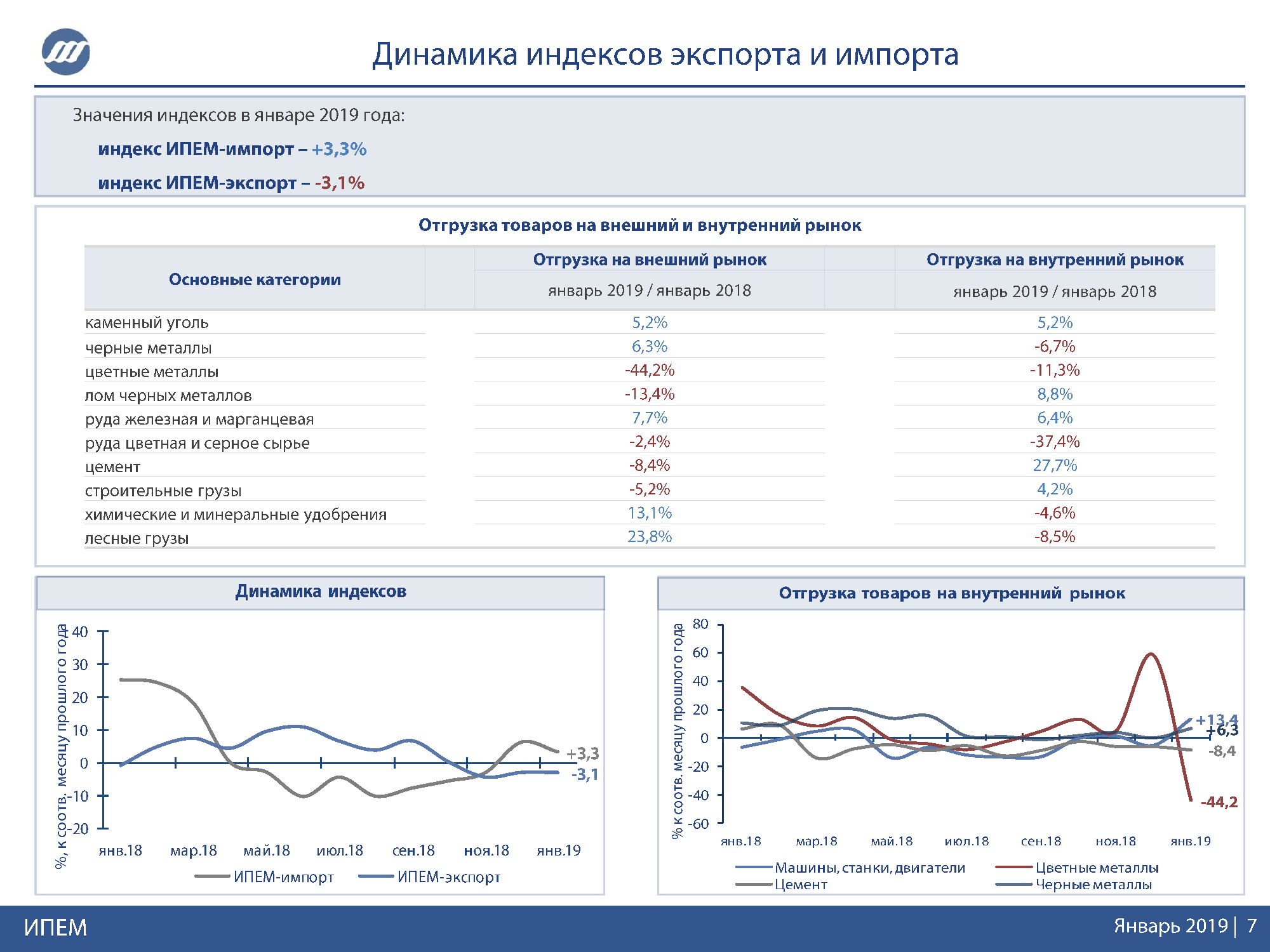 Синтез кДНК с использованием олиго (dT) праймера осуществляли с помощью набора RETROscript (Ambion). Эту кДНК использовали для количественного ПЦР-анализа в реальном времени генов Gag-Pol-CTE и ERK2 (эталон) с использованием специфических для генов праймеров. Результаты, полученные из данных ПЦР в реальном времени, представлены в виде значений CT, где CT определяется как пороговый номер цикла, при котором происходит обнаружение амплифицированного продукта.Среднее значение CT рассчитывали как для гена-мишени (Gag-Pol-CTE или Luc-CTE), так и для ERK2 (контроль), а ΔCT определяли как (среднее значение трех повторных значений CT для гена CTE) минус ( среднее значение трех повторных значений CT для ERK2 ). ΔΔCT представляет собой разницу между клетками с нокдауном Tpr и контрольными клетками, рассчитанную по формуле ΔΔCT = (ΔCT клеток с нокдауном Tpr — ΔCT контрольных клеток). N-кратная дифференциальная экспрессия целевого гена (Gag-Pol-CTE или Luc-CTE) в клетках, лишенных Tpr, по сравнению с контрольными клетками, трансфицированными NS-Si, выражалась как 2 -ΔΔCT [62].
Синтез кДНК с использованием олиго (dT) праймера осуществляли с помощью набора RETROscript (Ambion). Эту кДНК использовали для количественного ПЦР-анализа в реальном времени генов Gag-Pol-CTE и ERK2 (эталон) с использованием специфических для генов праймеров. Результаты, полученные из данных ПЦР в реальном времени, представлены в виде значений CT, где CT определяется как пороговый номер цикла, при котором происходит обнаружение амплифицированного продукта.Среднее значение CT рассчитывали как для гена-мишени (Gag-Pol-CTE или Luc-CTE), так и для ERK2 (контроль), а ΔCT определяли как (среднее значение трех повторных значений CT для гена CTE) минус ( среднее значение трех повторных значений CT для ERK2 ). ΔΔCT представляет собой разницу между клетками с нокдауном Tpr и контрольными клетками, рассчитанную по формуле ΔΔCT = (ΔCT клеток с нокдауном Tpr — ΔCT контрольных клеток). N-кратная дифференциальная экспрессия целевого гена (Gag-Pol-CTE или Luc-CTE) в клетках, лишенных Tpr, по сравнению с контрольными клетками, трансфицированными NS-Si, выражалась как 2 -ΔΔCT [62].
Дополнительная информация
Рисунок S1.
Роль Tpr в Rev-зависимом и CTE-опосредованном экспорте несплайсированной РНК. (A) Репортерную конструкцию Gag/PR-RRE вместе с плазмидами Flag-Rev и CMV-β-Gal котрансфицировали различными олигонуклеотидами Tpr siRNA, и через 48 часов лизаты анализировали на экспрессию p24. (B) Анализировали уровни β-галактозидазы в каждом из образцов. Столбцы представляют среднее значение полученных значений, а столбцы погрешностей представляют собой стандартное отклонение (s.г) значений, полученных при трех независимых трансфекциях. Соответствующие нормализованные значения p24 (по отношению к β-Gal) представлены на рисунке 3B. (C) Показания ELISA p24 клеточных экстрактов HEK293T, отражающие повышенные уровни продуктов расщепления белка Gag/Pol в клетках, собранных через 48 часов после трансфекции репортерной конструкцией Gag/Pol-CTE, CMV-β-Gal и различными миРНК Tpr. (D) Активность β-галактозидазы оценивается в каждом из образцов. Соответствующие нормализованные значения p24 представлены на рисунке 3D.
Соответствующие нормализованные значения p24 представлены на рисунке 3D.
https://doi.org/10.1371/journal.pone.0029921.s001
(TIF)
Рисунок S2.
Истощение Tpr вызывает усиление функции CTE в клетках млекопитающих. (A и B) Клетки HEK293T, COS-1 и HeLa трансфицировали либо NS-Si, либо TSi и Gag/Pol-CTE и репортерной конструкцией CMV-β-Gal, и лизаты анализировали на p24 (панель A) и β Экспрессия Gal (панель B) через 48 часов после трансфекции. Столбцы представляют собой среднее значение, а столбцы погрешностей представляют собой s.д. значений, полученных из трех независимых трансфекций. Соответствующие нормализованные значения p24 представлены на рисунке 4B. (C) Клетки HEK293T котрансфицировали конструкциями NS-Si или Tsi и CTE-Luc и CMV-β-Gal, а активность люциферазы в лизатах определяли через 48 часов после трансфекции. (D) Анализировали уровни β-галактозидазы в образцах. Соответствующие нормализованные показания люциферазы представлены на рисунке 4E.
https://doi.org/10.1371/journal.pone.0029921.s002
(ТИФ)
Рисунок S3.
Снижение уровней p24 наблюдается после восстановления с помощью устойчивого к siRNA клона Tpr. (A) Клетки HEK293T, временно трансфицированные конструкциями Flag-Tpr и Flag-Tpr-Si. (B и C) Конструкции Flag-Tpr или FLAG-Tpr-Si трансфицировали в клетки HEK293T вместе с NS-Si или TSi и репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal. Анализировали экспрессию p24 (панель B) и уровни β-галактозидазы (панель C) в каждом из образцов.Соответствующие нормализованные значения p24 представлены на рисунке 5D. (D и E) Клетки HEK293T, стабильно экспрессирующие Flag-Tpr или Flag-Tpr-Si, трансфицировали NS-Si или TSi вместе с плазмидами Gag/Pol-CTE и CMV-β-Gal. Клеточные лизаты анализировали на экспрессию p24 (панель D) и β-Gal (панель E). Соответствующие нормализованные значения p24 представлены на рисунке 5G.
https://doi.org/10.1371/journal.pone.0029921.s003
(TIF)
Рисунок S4.
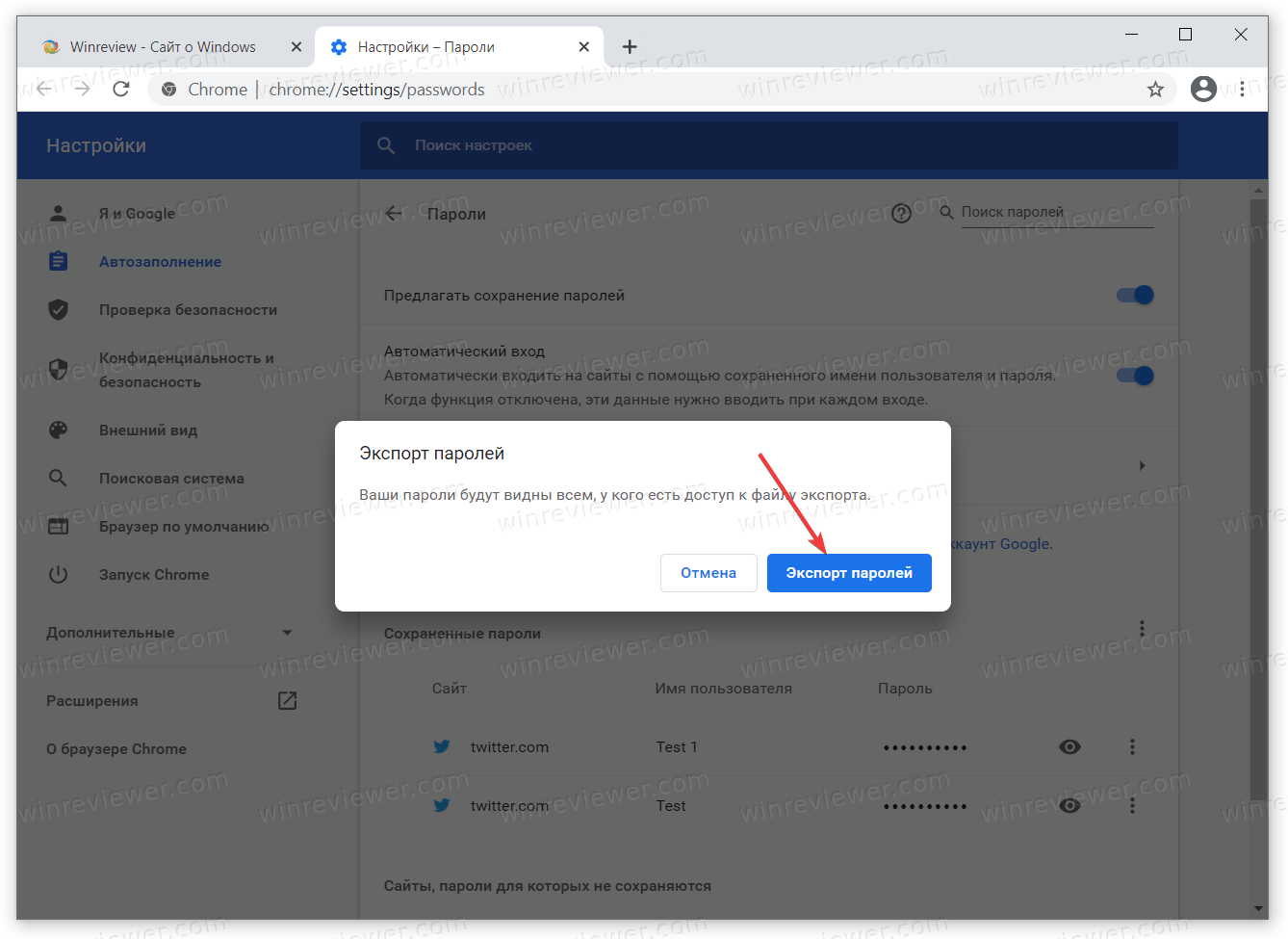
Регуляция экспорта несплайсированной РНК в клетках с нокдауном Tpr при комбинированном истощении или сверхэкспрессии белков Tap/Nxf1 и Sam68.Клетки (A и B) трансфицировали 1 мкг siRNA против Sam68 или Tap/Nxf1 вместе с NS-Si или TSi. Клетки повторно высевали на следующий день и через 24 часа после повторного посева клетки еще раз трансфицировали олигонуклеотидами siRNA и репортерными конструкциями. Через 48 часов после трансфекции анализировали экспрессию репортерного гена из трансфицированных конструкций Gag/Pol-CTE (панель A) и CMV-β-Gal (панель B). Соответствующие нормализованные значения представлены на рисунке 7B. (C и D) После 48 часов обработки NS-Si и TSi клетки HEK293T повторно трансфицировали теми же олигонуклеотидами siRNA вместе с плазмидами Gag/Pol-CTE и CMV-β-Gal и HA-Sam68 или HA-Tap. /Кxf1конструирует.Полученные таким образом лизаты анализировали на количество p24 (панель C) и экспрессию β-Gal (панель D). Данные представляют собой среднее значение, а планки погрешностей соответствуют стандартному отклонению.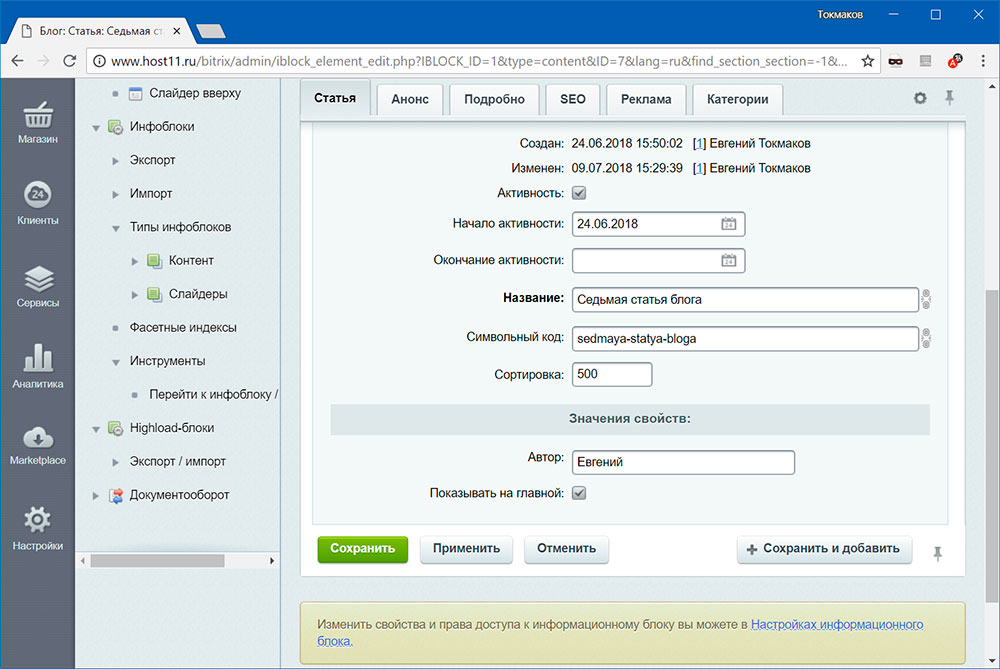 получен из трех независимых трансфекций. Соответствующие нормализованные значения представлены на рисунке 8B.
получен из трех независимых трансфекций. Соответствующие нормализованные значения представлены на рисунке 8B.
https://doi.org/10.1371/journal.pone.0029921.s004
(TIF)
Рисунок S5.
Истощение Nup153 также влияет на экспорт, зависящий от CTE. Клетки (А и В) HEK293T трансфицировали миРНК против различных нуклеопоринов вместе с конструкциями Gag/Pol-CTE и CMV-β-Gal.Через 48 часов после трансфекции в лизатах оценивали экспрессию p24 (панель A) и β-Gal (панель B). Соответствующие нормализованные значения представлены на рисунке 9B. (C и D) Клетки трансфицировали siРНК против Nup153 или Tpr или Nup153+Tpr вместе с конструкциями Gag/Pol-CTE и CMV-β-Gal. Уровни p24 (панель C) и показания β-галактозидазы (панель D), наблюдаемые в клетках, трансфицированных репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal вместе с TSi и/или Nup153-siRNA. Соответствующие нормализованные значения представлены на рисунке 9D.
https://doi.org/10.1371/journal. pone.0029921.s005
pone.0029921.s005
(TIF)
Рисунок S6.
N-концевая область Tpr необходима для регуляции CTE-опосредованного экспорта несплайсированной РНК. (A) Схематическое изображение различных фрагментов делеции Tpr. (B) Иммуноблот, изображающий экспрессию различных фрагментов делеции Tpr, помеченных Flag, в клетках, лишенных эндогенного Tpr. (C и D) уровни p24 (панель C) и показания β-галактозидазы (панель D), наблюдаемые в клетках, трансфицированных репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal вместе с TSi и спасенных с помощью различных делеционных конструкций белка .(E) Нормализованные значения p24 ELISA в клетках HEK293T, обработанных TSi в течение 48 часов и восстановленных с помощью различных делеционных конструкций белка. (F) Иммунофлуоресцентная микроскопия клеток, трансфицированных различными делеционными конструкциями Tpr.
https://doi.org/10.1371/journal.pone.0029921.s006
(TIF)
Рисунок S7.
Rescue с локализованно-дефицитным мутантом Tpr не приводит к снижению уровней p24. (A) Клетки HEK293T, временно трансфицированные конструкцией Flag-Tpr-L458P/M489P-Si.(B и C) Клетки котрансфицировали NS-Si или TSi или Nup153-siRNA вместе с репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal и устойчивым к Tpr-Si или siRNA локализационным мутантом Tpr (Tpr-L458P). /M489P-Si). Через 48 часов после трансфекции в лизатах оценивали количество экспрессии p24 и β-Gal. Соответствующие нормализованные значения представлены на фигуре 10C.
(A) Клетки HEK293T, временно трансфицированные конструкцией Flag-Tpr-L458P/M489P-Si.(B и C) Клетки котрансфицировали NS-Si или TSi или Nup153-siRNA вместе с репортерными конструкциями Gag/Pol-CTE и CMV-β-Gal и устойчивым к Tpr-Si или siRNA локализационным мутантом Tpr (Tpr-L458P). /M489P-Si). Через 48 часов после трансфекции в лизатах оценивали количество экспрессии p24 и β-Gal. Соответствующие нормализованные значения представлены на фигуре 10C.
https://doi.org/10.1371/journal.pone.0029921.s007
(TIF)
Рисунок S8.
Нуклеопорин Tpr не взаимодействует с белками Tap/Nxf1 и Sam68. (A) Клетки трансфицировали конструкциями HA-ERK2, HA-Sam68, HA-Nxt/p15 или HA-Tap/Nxf1. Через 24 часа после трансфекции клетки лизировали и лизаты подвергали иммунопреципитации с НА-антителами. Иммуноблоты исследовали антителами против HA и против Tpr для определения взаимодействий между Tpr и белками, мечеными HA. Ко-иммунопреципитация эндогенного Tpr вместе с HA-ERK2 подтверждает правильность подхода.
https://doi.org/10.1371/journal.pone.0029921.s008
(TIF)
Благодарности
Мы благодарим доктора.Майклу Дж. Веберу за его поддержку, предложения и критическое прочтение рукописи. Мы благодарим доктора Мари-Лузи Хаммаршельд и доктора Джона Койла за предоставленные материалы. Мы благодарим центральную конфокальную микроскопию НИИ. Мы благодарим Аншука Саркара за его помощь в создании стабильных клеточных линий Flag-Tpr и Flag-Tpr-Si; Д-р Ханс-Георг Крауслих (Гейдельбергский университет, Германия), д-р Джомон Джозеф (NCCS, Пуна), д-р Сагар Сенгупта, д-р А.С.Банерджа и д-р Суданшу Врати (НИИ, Нью-Дели) за предоставленные материалы.
Авторские взносы
Идея и разработка экспериментов: КР ВКН. Выполняли опыты: КР. Проанализированы данные: КР ВКН. Написал газету: КР ВКН.
Каталожные номера
- 1.
Греко А., Пьеротти М.А., Бонгарзоне И., Пальярдини С., Ланци С. и др. (1992) TRK-T1 представляет собой новый онкоген, образованный слиянием генов TPR и TRK в папиллярных карциномах щитовидной железы человека.
 Онкоген 7: 237–242.
Онкоген 7: 237–242. - 2. Парк М., Дин М., Купер С.С., Шмидт М., О’Брайен С.Дж. и др.(1986) Механизм активации метонкогена. Ячейка 45: 895–904.
- 3. Соман Н.Р., Корреа П., Руис Б.А., Воган Г.Н. (1991) Онкогенная перестройка TPR-MET присутствует и экспрессируется в карциноме желудка человека и предшествующих поражениях. Proc Natl Acad Sci U S A 88: 4892–4896.
- 4. Mitchell PJ, Cooper CS (1992) Ген tpr человека кодирует белок из 2094 аминокислот, который имеет обширные спиральные области и кислый С-концевой домен. Онкоген 7: 2329–2333.
- 5. Cordes VC, Reidenbach S, Rackwitz HR, Franke WW (1997)Идентификация белка p270/Tpr в качестве составного компонента внутриядерных нитей, прикрепленных к комплексу ядерных пор. J Cell Biol 136: 515–529.
- 6.
Shah S, Tugendreich S, Forbes D (1998) Основными сайтами связывания ядерного импортного рецептора являются внутренний нуклеопорин Nup153 и соседний белок ядерной нити Tpr.
 J Cell Biol 141: 31–49.
J Cell Biol 141: 31–49. - 7. Hase ME, Cordes VC (2003)Прямое взаимодействие с nup153 опосредует связывание Tpr с периферией комплекса ядерных пор.Мол Биол Ячейка 14: 1923–1940.
- 8. Кузнецов Н.В., Сандблад Л., Хасе М.Е., Хунцикер А., Хергт М. и др. (2002) Эволюционно консервативный однокопийный ген мышиного Tpr кодирует одну преобладающую изоформу в соматических клетках и не имеет паралогов у высших эукариот. Хромосома 111: 236–255.
- 9. Косова Б., Панте Н., Ролленхаген С., Подтележников А., Манн М. и др. (2000) Mlp2p, компонент внутриядерных филаментов, прикрепленных к ядерной поре, ассоциирован с nic96p.J Biol Chem 275: 343–350.
- 10. Strambio-de-Castillia C, Blobel G, Rout MP (1999) Белки, соединяющие комплекс ядерных пор с внутренней частью ядра. J Cell Biol 144: 839–855.
- 11.
Fontoura BM, Dales S, Blobel G, Zhong H (2001)Нуклеопорин Nup98 связан с внутриядерной нитевидной белковой сетью TPR.
 Proc Natl Acad Sci U S A 98: 3208–3213.
Proc Natl Acad Sci U S A 98: 3208–3213. - 12. Frosst P, Guan T, Subauste C, Hahn K, Gerace L (2002) Tpr локализован в ядерной корзине порового комплекса и играет роль в экспорте ядерных белков.J Cell Biol 156: 617–630.
- 13. Shibata S, Matsuoka Y, Yoneda Y (2002)Нуклеоцитоплазматический транспорт белков и поли(A)+ РНК в реконструированных ядрах без Tpr в живых клетках млекопитающих. Гены Клетки 7: 421–434.
- 14. Зимовска Г., Пэдди М.Р. (2002) Структуры и динамика Tpr дрозофилы, несовместимые со статической нитевидной структурой. Разрешение ячейки опыта 276: 223–232.
- 15. Cornett J, Cao F, Wang CE, Ross CA, Bates GP, et al.(2005)Полиглутаминовое расширение гентингтина ухудшает его ядерный экспорт. Нат Жене 37: 198–204.
- 16.
Lee SH, Sterling H, Burlingame A, McCormick F (2008) Tpr непосредственно связывается с Mad1 и Mad2 и важен для Mad1-Mad2-опосредованной контрольной точки митотического веретена.
 Гены Дев 22: 2926–2931.
Гены Дев 22: 2926–2931. - 17. Nakano H, Funasaka T, Hashizume C, Wong RW (2010)Транслоцированная промоторная область нуклеопорина (Tpr) связывается с динеиновым комплексом, предотвращая образование отставания хромосом во время митоза.J Biol Chem 285: 10841–10849.
- 18. Xu XM, Rose A, Muthuswamy S, Jeong SY, Venkatakrishnan S, et al. (2007) NUCLEAR PORE ANCHOR, гомолог Tpr/Mlp1/Mlp2/megator арабидопсиса, участвует в экспорте мРНК и гомеостазе SUMO и влияет на различные аспекты развития растений. Заводская ячейка 19: 1537–1548.
- 19. Jacob Y, Mongkolsiriwatana C, Veley KM, Kim SY, Michaels SD (2007) Белок ядерной поры AtTPR необходим для гомеостаза РНК, времени цветения и передачи сигналов ауксина.Завод Физиол 144: 1383–1390.
- 20. Skaggs HS, Xing H, Wilkerson DC, Murphy LA, Hong Y, et al. (2007) Взаимодействие HSF1-TPR способствует экспорту стресс-индуцированной мРНК HSP70. J Biol Chem 282: 33902–33907.
- 21.
 Эблен С.Т., Кумар Н.В., Шах К., Хендерсон М.Дж., Уоттс С.К. и др. (2003)Идентификация новых субстратов ERK2 с помощью сконструированной киназы и аналогов АТФ. J Biol Chem 278: 14926–14935.
Эблен С.Т., Кумар Н.В., Шах К., Хендерсон М.Дж., Уоттс С.К. и др. (2003)Идентификация новых субстратов ERK2 с помощью сконструированной киназы и аналогов АТФ. J Biol Chem 278: 14926–14935. - 22. Vomastek T, Iwanicki MP, Burack WR, Tiwari D, Kumar D, et al.(2008) Сайты фосфорилирования внеклеточной регулируемой сигналом киназы 2 (ERK2) и стыковочный домен на белке комплекса ядерной поры Tpr совместно регулируют взаимодействие ERK2-Tpr. Мол Селл Биол 28: 6954–6966.
- 23. Cochrane AW, Chen CH, Rosen CA (1990)Специфическое взаимодействие белка Rev вируса иммунодефицита человека со структурированной областью в мРНК env. Proc Natl Acad Sci U S A 87: 1198–1202.
- 24. Malim MH, Hauber J, Fenrick R, Cullen BR (1988)Транс-активатор вируса иммунодефицита rev модулирует экспрессию вирусных регуляторных генов.Природа 335: 181–183.
- 25.
Askjaer P, Jensen TH, Nilsson J, Englmeier L, Kjems J (1998) Специфичность взаимодействия ядерного экспортного сигнала CRM1-Rev опосредована RanGTP.
 J Biol Chem 273: 33414–33422.
J Biol Chem 273: 33414–33422. - 26. Coyle JH, Guzik BW, Bor YC, Jin L, Eisner-Smerage L, et al. (2003) Sam68 усиливает цитоплазматическое использование интрон-содержащей РНК и функционально регулируется ядерной киназой Sik/BRK. Мол Селл Биол 23: 92–103.
- 27.Паскинелли А.Е., Эрнст Р.К., Лунд Э., Гримм С., Запп М.Л. и соавт. (1997) Конститутивный транспортный элемент (CTE) обезьяньего вируса Mason-Pfizer (MPMV) получает доступ к пути экспорта клеточной мРНК. EMBO J 16: 7500–7510.
- 28. Бэнгс П., Берк Б., Пауэрс С., Крейг Р., Пурохит А. и др. (1998) Функциональный анализ Tpr: идентификация ассоциации комплекса ядерных пор и доменов ядерной локализации и роли в экспорте мРНК. J Cell Biol 143: 1801–1812.
- 29.Лав Д.К., Свейцер Т.Д., Ганновер Дж.А. (1998)Реконструкция ядерного экспорта ВИЧ-1 rev: независимые требования к ядерному импорту и экспорту. Proc Natl Acad Sci U S A 95: 10608–10613.
- 30.
Гали В., Гадаль О.
 , Фромонт-Расин М., Романо А., Жакье А. и др. (2004) Ядерное удержание несплайсированных мРНК у дрожжей опосредуется перинуклеарным Mlp1. Ячейка 116: 63–73.
, Фромонт-Расин М., Романо А., Жакье А. и др. (2004) Ядерное удержание несплайсированных мРНК у дрожжей опосредуется перинуклеарным Mlp1. Ячейка 116: 63–73. - 31. Smith AJ, Cho MI, Hammarskjold ML, Rekosh D (1990) Вирус иммунодефицита человека типа 1 Pr55gag и Pr160gag-pol, экспрессируемые из обезьяньего вируса 40 позднего замещающего вектора, эффективно процессируются и собираются в вирусоподобные частицы.Дж. Вирол 64: 2743–2750.
- 32. Шринивасакумар Н., Хаммаршельд М.Л., Рекош Д. (1995) Характеристика делеционных мутаций в области капсида вируса иммунодефицита человека типа 1, которые влияют на образование частиц и включение предшественника Gag-Pol. Дж. Вирол 69: 6106–6114.
- 33. Wodrich H, Schambach A, Krauslich HG (2000) Множественные копии конститутивного транспортного элемента РНК вируса обезьян Mason-Pfizer приводят к усиленной экспрессии Gag ВИЧ-1 контекстно-зависимым образом.Нуклеиновые кислоты, рез. 28: 901–910.
- 34.
 Jin L, Guzik BW, Bor YC, Rekosh D, Hammarskjold ML (2003) Tap и NXT способствуют трансляции несплайсированных мРНК. Гены Дев 17: 3075–3086.
Jin L, Guzik BW, Bor YC, Rekosh D, Hammarskjold ML (2003) Tap и NXT способствуют трансляции несплайсированных мРНК. Гены Дев 17: 3075–3086. - 35. Vinciguerra P, Iglesias N, Camblong J, Zenklusen D, Stutz F (2005) Перинуклеарные белки Mlp подавляют экспрессию генов в ответ на дефект экспорта мРНК. EMBO J 24: 813–823.
- 36. Reddy TR, Tang H, Xu W, Wong-Staal F (2000) Sam68, РНК-хеликаза A и Tap взаимодействуют в посттранскрипционной регуляции вируса иммунодефицита человека и мРНК ретровируса типа D.Онкоген 19: 3570–3575.
- 37. Herold A, Klymenko T, Izaurralde E (2001) Гетеродимеры NXF1/p15 необходимы для ядерного экспорта мРНК у Drosophila. РНК 7: 1768–1780.
- 38. Herold A, Suyama M, Rodrigues JP, Braun IC, Kutay U, et al. (2000) TAP (NXF1) принадлежит к мультигенному семейству предполагаемых факторов экспорта РНК с консервативной модульной архитектурой. Мол Селл Биол 20: 8996–9008.
- 39.
 Левеск Л., Бор Ю.С., Мацат Л.Х., Джин Л., Бербероглу С. и др.(2006) Мутации в tap разъединяют экспортную активность РНК от транслокации через комплекс ядерных пор. Мол Биол Ячейка 17: 931–943.
Левеск Л., Бор Ю.С., Мацат Л.Х., Джин Л., Бербероглу С. и др.(2006) Мутации в tap разъединяют экспортную активность РНК от транслокации через комплекс ядерных пор. Мол Биол Ячейка 17: 931–943. - 40. Katahira J, Inoue H, Hurt E, Yoneda Y (2009)Адаптер Aly и коадаптер Thoc5 функционируют в опосредованном Tap-p15 ядерном экспорте мРНК HSP70. EMBO J 28: 556–567.
- 41. Пембертон Л.Ф., Пасхал Б.М. (2005)Механизмы опосредованного рецептором ядерного импорта и ядерного экспорта. Трафик 6: 187–198.
- 42. Крулл С., Доррис Дж., Бойсен Б., Райденбах С., Магниус Л. и др.(2010) Белок Tpr необходим для установления зон исключения гетерохроматина, связанных с ядерными порами. EMBO J 29: 1659–1673.
- 43.
Кокрейн А.В., Перкинс А., Розен К.А. (1990)Идентификация последовательностей, важных для ядрышковой локализации вируса иммунодефицита человека Rev: значение ядрышковой локализации для функции. Дж. Вирол 64: 881–885.

- 44. Эрнст Р.К., Брей М., Рекош Д., Хаммаршельд М.Л. (1997)Структурированный элемент ретровирусной РНК, который обеспечивает ядерно-цитоплазматический экспорт интрон-содержащей РНК.Мол Селл Биол 17: 135–144.
- 45. Kang Y, Bogerd HP, Cullen BR (2000) Анализ клеточных факторов, которые опосредуют ядерный экспорт РНК, несущих конститутивный транспортный элемент вируса обезьян Mason-Pfizer. Дж. Вирол 74: 5863–5871.
- 46. Wiegand HL, Coburn GA, Zeng Y, Kang Y, Bogerd HP, et al. (2002) Формирование гетеродимеров Tap/NXT1 активирует Tap-зависимый экспорт ядерной мРНК путем усиления рекрутирования в комплексы ядерных пор. Мол Селл Биол 22: 245-256.
- 47. Левеск Л., Гузик Б., Гуан Т., Койл Дж., Блэк Б.Е. и др. (2001) Экспорт РНК, опосредованный tap, включает NXT1-зависимые взаимодействия с комплексом ядерной поры. J Biol Chem 276: 44953–44962.
- 48.
Skruzny M, Schneider C, Racz A, Weng J, Tollervey D, et al.
 (2009)Эндорибонуклеаза, функционально связанная с контролем качества околоядерных мРНП, связана с комплексами ядерных пор. ПЛОС Биол 7: e8.
(2009)Эндорибонуклеаза, функционально связанная с контролем качества околоядерных мРНП, связана с комплексами ядерных пор. ПЛОС Биол 7: e8. - 49. Охниси Т., Ямасита А., Кашима И., Шелл Т., Андерс К.Р. и др.(2003) Фосфорилирование hUPF1 индуцирует образование комплексов наблюдения мРНК, содержащих hSMG-5 и hSMG-7. Мол Ячейка 12: 1187–1200.
- 50. Unterholzner L, Izaurralde E (2004) SMG7 действует как молекулярная связь между наблюдением за мРНК и распадом мРНК. Мол Ячейка 16: 587–596.
- 51. Glavan F, Behm-Ansmant I, Izaurralde E, Conti E (2006) Структуры PIN-доменов SMG6 и SMG5 обнаруживают нуклеазу в комплексе наблюдения за мРНК. EMBO J 25: 5117–5125.
- 52. Terry LJ, Wente SR (2007) Экспорт ядерной мРНК требует специфических нуклеопоринов FG для транслокации через комплекс ядерных пор. J Cell Biol 178: 1121–1132.
- 53.
Lei EP, Silver PA (2002)Экспорт белков и РНК из ядра. Ячейка разработчиков 2: 261–272.

- 54. Weis K (2003)Регулирование доступа к геному: ядерно-цитоплазматический транспорт на протяжении клеточного цикла. Ячейка 112: 441–451.
- 55. Powers MA, Forbes DJ, Dahlberg JE, Lund E (1997) Нуклеопорин GLFG позвоночных, Nup98, является важным компонентом множественных путей экспорта РНК.J Cell Biol 136: 241–250.
- 56. Ren Y, Seo HS, Blobel G, Hoelz A (2010)Структурный и функциональный анализ взаимодействия между нуклеопорином Nup98 и фактором экспорта мРНК Rae1. Proc Natl Acad Sci U S A 107: 10406–10411.
- 57. Mackay DR, Elgort SW, Ullman KS (2009)Нуклеопорин Nup153 играет отдельные роли как в ранней митотической прогрессии, так и в разрешении митоза. Мол Биол Ячейка 20: 1652–1660.
- 58. Bastos R, Lin A, Enarson M, Burke B (1996)Нацеливание и функция в экспорте мРНК белка Nup153 комплекса ядерных пор.J Cell Biol 134: 1141–1156.
- 59.
Ульман К.С., Шах С., Пауэрс М.
 А., Forbes DJ (1999) Нуклеопорин nup153 играет критическую роль во многих типах ядерного экспорта. Мол Биол Селл 10: 649–664.
А., Forbes DJ (1999) Нуклеопорин nup153 играет критическую роль во многих типах ядерного экспорта. Мол Биол Селл 10: 649–664. - 60. Coyle JH, Bor YC, Rekosh D, Hammarskjold ML (2011) Белок Tpr регулирует экспорт мРНК с сохраненными интронами, которые проходят через путь Nxf1. РНК.
- 61. Lin Q, Taylor SJ, Shalloway D (1997) Специфичность и детерминанты связывания РНК Sam68.Последствия для биологической функции доменов гомологии K. J Biol Chem 272: 27274–27280.
- 62. Livak KJ, Schmittgen TD (2001) Анализ данных об относительной экспрессии генов с использованием количественной ПЦР в реальном времени и метода 2(-Delta Delta C(T)). Методы 25: 402–408.
Мы не можем найти эту страницу
(* {{l10n_strings.REQUIRED_FIELD}})
{{l10n_strings.CREATE_NEW_COLLECTION}}*
{{l10n_strings.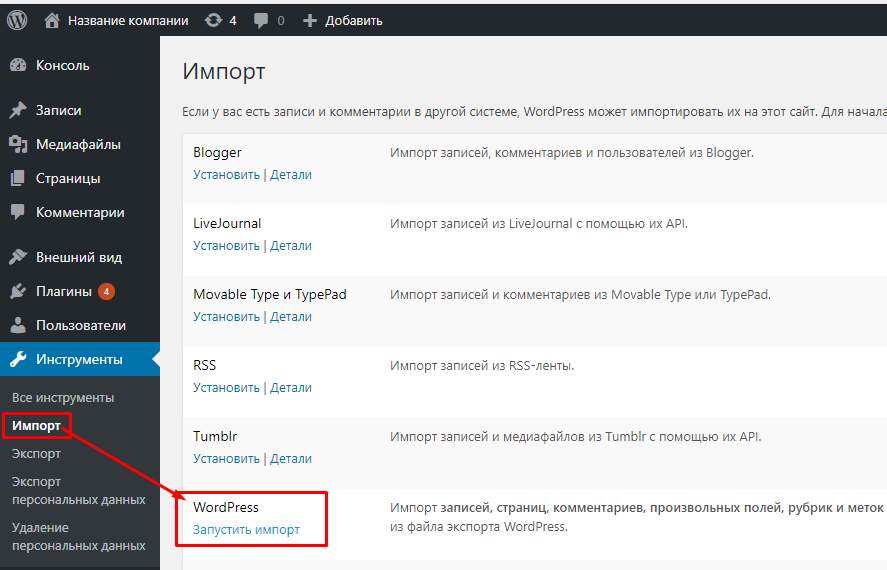 ADD_COLLECTION_DESCRIPTION}}
ADD_COLLECTION_DESCRIPTION}}
{{l10n_strings.DRAG_TEXT_HELP}}
{{l10n_strings.LANGUAGE}} {{$select.selected.display}} {{статья.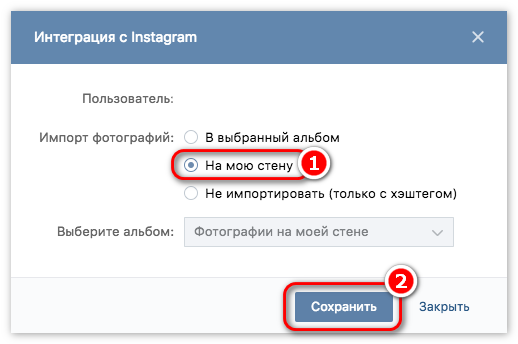 content_lang.display}}
content_lang.display}}
{{l10n_strings.AUTHOR_TOOLTIP_TEXT}}
{{$выбрать.выбранный.дисплей}} {{l10n_strings.CREATE_AND_ADD_TO_COLLECTION_MODAL_BUTTON}} {{l10n_strings.CREATE_A_COLLECTION_ERROR}}Огромный рост экспорта медицинского масла каннабиса из Канады в 2019 году
В 2019 году было зафиксировано огромное увеличение экспорта канадского масла каннабиса в медицинских целях в Европу. 3 литра в 2019 году.
3 литра в 2019 году.
Австралия и Европа были двумя основными экспортными рынками.
21% всего экспортируемого масла было отгружено в Германию и Данию объемом 790 литров и 336 литров соответственно. Масла медицинского каннабиса поставлялись дополнительно более чем в 10 других стран.
Согласно данным Министерства здравоохранения Канады, в 2019 году продуктов из масла каннабиса были одобрены для экспорта как минимум в 17 стран для медицинских и научных целей.
Министерство здравоохранения Канады одобрило около 12 887.86 литров нефтепродуктов каннабиса на экспорт в 2019 году, но фактические поставки на конец года достигли 50% от утвержденного количества.
Это не обязательно означает, что оставшееся количество не было экспортировано, так как всегда существует задержка между выдачей разрешения на экспорт и моментом экспорта.
Факты о нефтепродуктах
- Рост экспорта масла медицинского каннабиса продолжал опережать рост экспорта сушеного каннабиса.

- В 2019 году Канада экспортировала почти вдвое больше масла каннабиса (5 372,3 литра, что эквивалентно 4 996 кг) по сравнению с количеством сушеных цветков каннабиса (3 740 кг) экспорт увеличился более чем в пять раз за тот же период.
- Массовый экспорт затронул несколько стран, что свидетельствует о том, что коммерциализировать экспорт медицинского каннабиса в больших количествах по-прежнему легче сказать, чем сделать.
Такие страны, как Австралия, Колумбия, Ямайка и Португалия, готовятся выйти на экспортный рынок.Существует убеждение, что масло становится все более привлекательным для других стран для использования в медицинских целях, поскольку люди не всегда хотят вдыхать сушеный каннабис, и что существует более широкий рынок, более высокая цена и легче импортировать и экспортировать масло медицинского каннабиса. продукты. Кроме того, в некоторых странах по-прежнему отсутствует производство сушеных цветов и масляных продуктов (Германия, Италия и т. д. ), поэтому они будут искать другие страны, чтобы получить эти продукты.
), поэтому они будут искать другие страны, чтобы получить эти продукты.
VK PREMIUM помогает инвесторам успешно производить нефтепродукты с высоким содержанием ТГК и помогает им поймать волну.
Мы предлагаем расширенный спектр консультационных услуг для содействия инвестициям в медицинский каннабис в Греции, включая стратегию и планирование, портфель продуктов с учетом текущих и будущих тенденций рынка, лицензирование, гранты с использованием Закона о стимулировании инвестиций, проектирование и строительство объекта в соответствии с Стандарты ЕС GMP и GACP и стратегии дистрибуции для обеспечения успеха продаж на зарубежных рынках.
Свяжитесь с нами
Мы всегда готовы обсудить ваш проект медицинского каннабиса.
Позвоните нам по телефону: +30 2106835560, отправьте электронное письмо по адресу: info[@]vkmedicalcannabis. com или заполните форму ниже:
com или заполните форму ниже:
Британские производители экспортируют излишки аппаратов ИВЛ | Производственный сектор
Британские производители должны экспортировать излишки аппаратов ИВЛ после того, как они произвели 14 000 аппаратов для лечения пациентов с коронавирусом, но обнаруживают, что большинство из них не нужны.
Борис Джонсон приветствовал успех «вызова вентиляторов», который начался в середине марта, когда он призвал британскую промышленность помочь произвести до 30 000 устройств на фоне опасений, что поставки NHS могут быть перегружены.
«Благодаря этим усилиям каждый, кто нуждался в аппарате ИВЛ, получил к нему доступ, а у NHS есть жизненно важные машины, необходимые для продолжения оказания жизненно важной поддержки в борьбе с этим смертельным вирусом», — сказал он.
Официальные данные показывают, что занятость аппаратов искусственной вентиляции легких достигла пика в 3301 в апреле. Запас аппаратов ИВЛ в Великобритании до пандемии составлял почти 9000 штук.
Премьер-министр потребовал 30 000 машин после того, как раннее научное моделирование, основанное на данных из Китая, показало, что для лечения пациентов с Covid-19 потребуется огромное количество машин.
Министр здравоохранения Мэтт Хэнкок позже снизил цель до 18 000 человек. Но меры социального дистанцирования и осознание врачами того, что менее инвазивные методы вентиляции предпочтительнее, означали, что количество устройств, доступных в NHS до пандемии, было достаточным.
Кабинет министров заявил в пятницу, что производство вентиляторов остановлено и что ведущая модель, произведенная специализированной фирмой Penlon, получила разрешение на экспорт.
Четыре различных устройства были одобрены для производства во время работы, что увеличило поставки в Великобритании до 25 000.
Кабинет министров заявил, что независимое тестирование показало, что можно было бы использовать еще четыре конструкции, включая CoVent производства Dyson.
Доктор Том Клаттон-Брок, директор центра тестирования и оценки медицинских устройств, который тестировал устройства, сказал: «Разработка, производство и тестирование аппаратов ИВЛ обычно занимают годы.



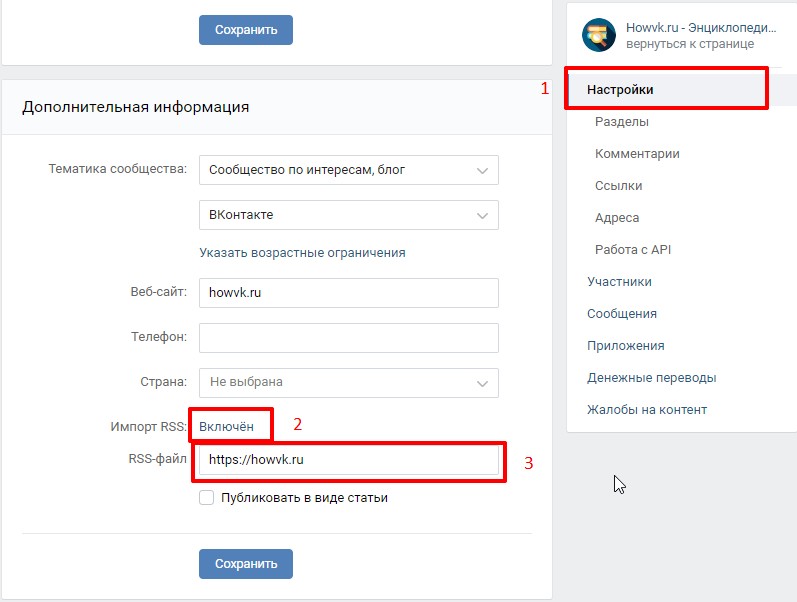

 exim.gov в разделе «Применить»), чтобы определить комиссионные сборы (премии).
exim.gov в разделе «Применить»), чтобы определить комиссионные сборы (премии).
 в Графике ограничений по странам, размещенном на веб-сайте Банка в разделе «Применить»).
в Графике ограничений по странам, размещенном на веб-сайте Банка в разделе «Применить»). Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie. Онкоген 7: 237–242.
Онкоген 7: 237–242. J Cell Biol 141: 31–49.
J Cell Biol 141: 31–49. Гены Дев 22: 2926–2931.
Гены Дев 22: 2926–2931.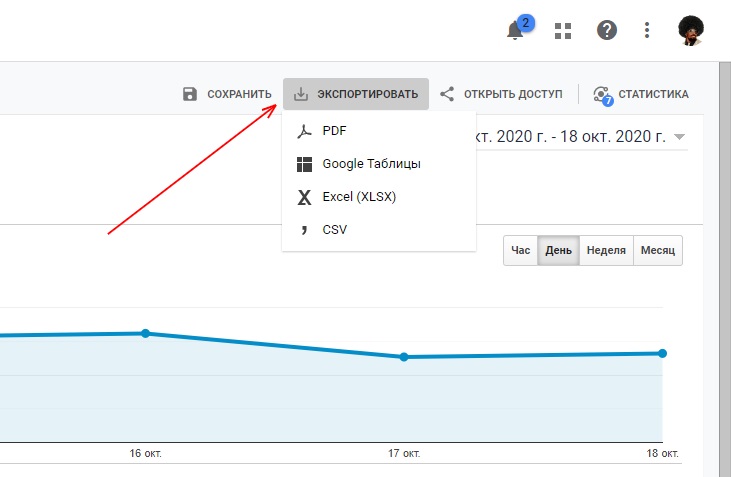 Эблен С.Т., Кумар Н.В., Шах К., Хендерсон М.Дж., Уоттс С.К. и др. (2003)Идентификация новых субстратов ERK2 с помощью сконструированной киназы и аналогов АТФ. J Biol Chem 278: 14926–14935.
Эблен С.Т., Кумар Н.В., Шах К., Хендерсон М.Дж., Уоттс С.К. и др. (2003)Идентификация новых субстратов ERK2 с помощью сконструированной киназы и аналогов АТФ. J Biol Chem 278: 14926–14935.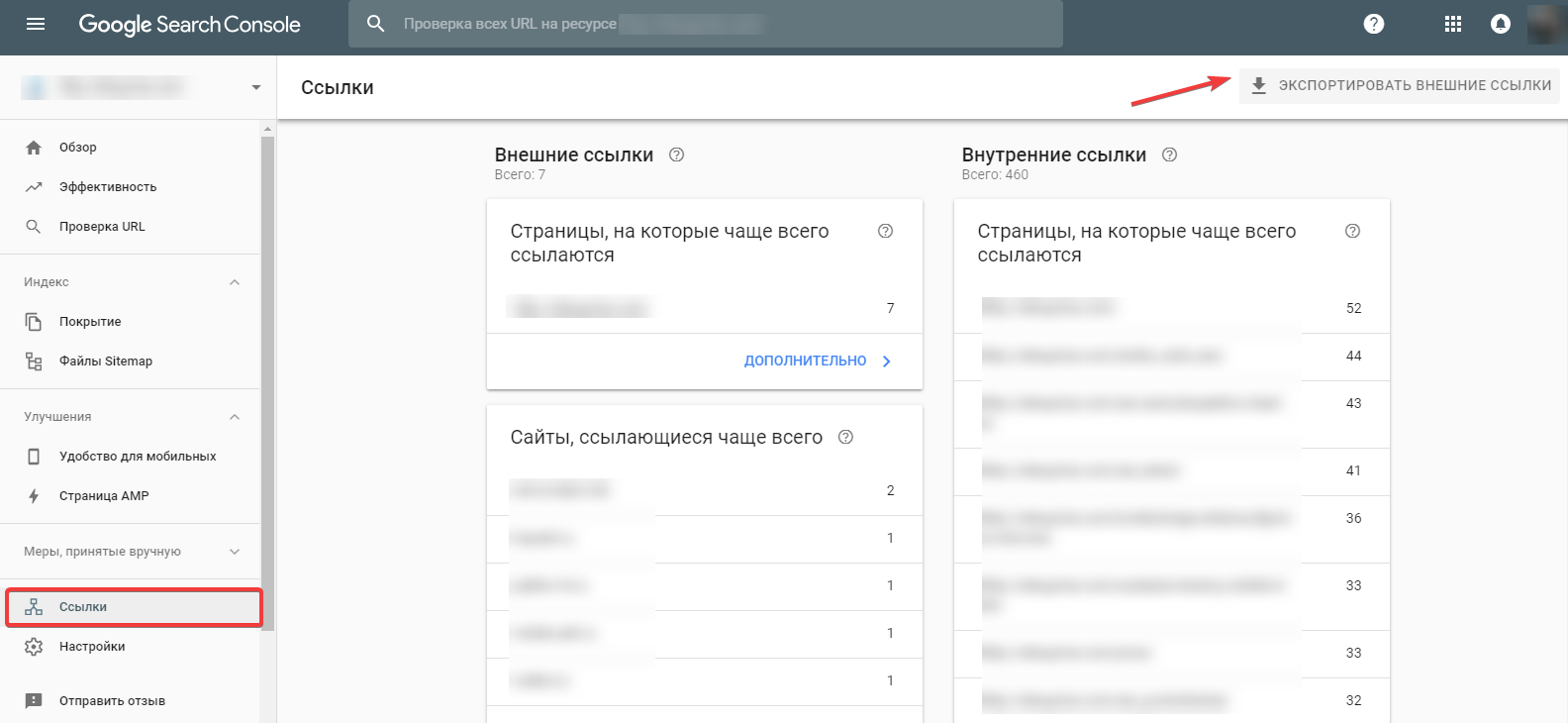 J Biol Chem 273: 33414–33422.
J Biol Chem 273: 33414–33422.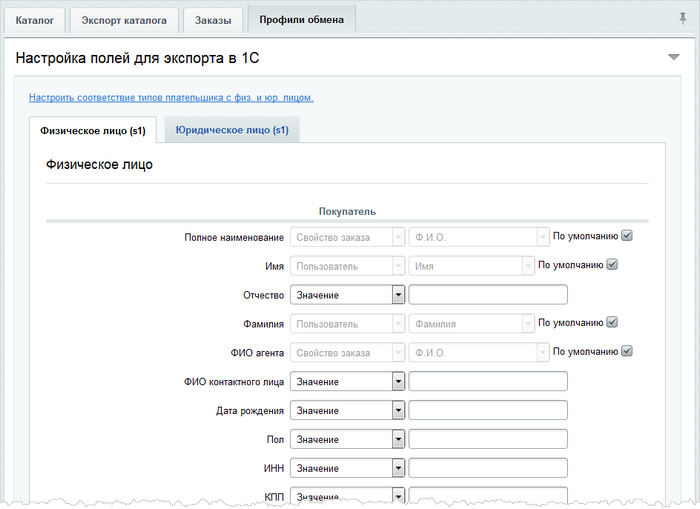 , Фромонт-Расин М., Романо А., Жакье А. и др. (2004) Ядерное удержание несплайсированных мРНК у дрожжей опосредуется перинуклеарным Mlp1. Ячейка 116: 63–73.
, Фромонт-Расин М., Романо А., Жакье А. и др. (2004) Ядерное удержание несплайсированных мРНК у дрожжей опосредуется перинуклеарным Mlp1. Ячейка 116: 63–73. Jin L, Guzik BW, Bor YC, Rekosh D, Hammarskjold ML (2003) Tap и NXT способствуют трансляции несплайсированных мРНК. Гены Дев 17: 3075–3086.
Jin L, Guzik BW, Bor YC, Rekosh D, Hammarskjold ML (2003) Tap и NXT способствуют трансляции несплайсированных мРНК. Гены Дев 17: 3075–3086.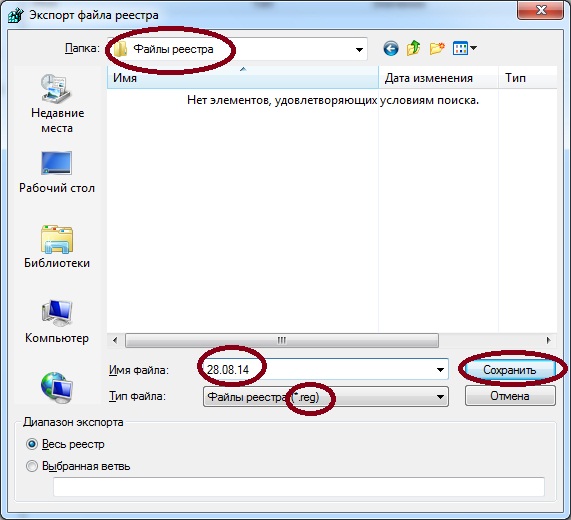 Левеск Л., Бор Ю.С., Мацат Л.Х., Джин Л., Бербероглу С. и др.(2006) Мутации в tap разъединяют экспортную активность РНК от транслокации через комплекс ядерных пор. Мол Биол Ячейка 17: 931–943.
Левеск Л., Бор Ю.С., Мацат Л.Х., Джин Л., Бербероглу С. и др.(2006) Мутации в tap разъединяют экспортную активность РНК от транслокации через комплекс ядерных пор. Мол Биол Ячейка 17: 931–943. (2009)Эндорибонуклеаза, функционально связанная с контролем качества околоядерных мРНП, связана с комплексами ядерных пор. ПЛОС Биол 7: e8.
(2009)Эндорибонуклеаза, функционально связанная с контролем качества околоядерных мРНП, связана с комплексами ядерных пор. ПЛОС Биол 7: e8.
 А., Forbes DJ (1999) Нуклеопорин nup153 играет критическую роль во многих типах ядерного экспорта. Мол Биол Селл 10: 649–664.
А., Forbes DJ (1999) Нуклеопорин nup153 играет критическую роль во многих типах ядерного экспорта. Мол Биол Селл 10: 649–664.